お知らせ
FOCUS:せん妄診療 up-to-date
◉高齢者の不眠を診る際,せん妄予防の視点が不可欠。
◉せん妄予防には,せん妄の病態機序の理解が必要。
◉せん妄の予防は,生命予後,転倒・転落,認知症発症,医療経済負担など,多岐にわたって好ましい影響をもたらす。
◉せん妄高リスク患者の予測に関する生物学的検討は進展中。
◉せん妄予防の非薬物的介入は,既に社会実装されている。
◉薬理学的なせん妄予防介入は進展中であり,中でもメラトニン受容体作動薬およびオレキシン受容体拮抗薬が有用。
◉せん妄の治療は,少数の二重盲検ランダム化比較試験に基づくより,薬理学的特性を勘案したエキスパートによるアルゴリズムのほうが現時点では有用。

❶ はじめに
せん妄は,高齢人口が著しく増加する状況で,一般病院の入院患者に最も頻繁に発症する精神疾患(精神状態)である。しかし,一般病院の1割程度にしか常勤精神科医が配置されておらず,その常勤精神科医の多くが外来業務に忙殺される中,非専門医がせん妄対応能力を習得することは必須と言える。
では,せん妄はなぜ問題となるのか。まず,患者自身の苦痛が強い。そして,看護・介護者の負担が著しく増加する。これらは,日常臨床から想像可能なことであろう。しかし,それだけではない。せん妄が大きな問題となるのは,転倒骨折のリスクを高め,身体疾患の重症度を上げ,その後の認知症発症やフレイルを促進し,生命予後に関わるなど,重大なアウトカムに影響するからである。そのため,医療費を上昇させて社会資源への負担を増大させる。それにもかかわらず「せん妄治療薬」として適応を獲得している薬剤がないという,精神医学のみならず医学全般の立ち遅れた課題なのである。
このような背景をふまえて,本稿では一般臨床医を対象として,最新のせん妄臨床を実務に沿って概説する。せん妄の臨床は10年前とはかなり異なるため,経験豊富な臨床医にとってもブラッシュアップに役立てばと思う。
❷ せん妄の概念と病態機序
(1) せん妄の概念
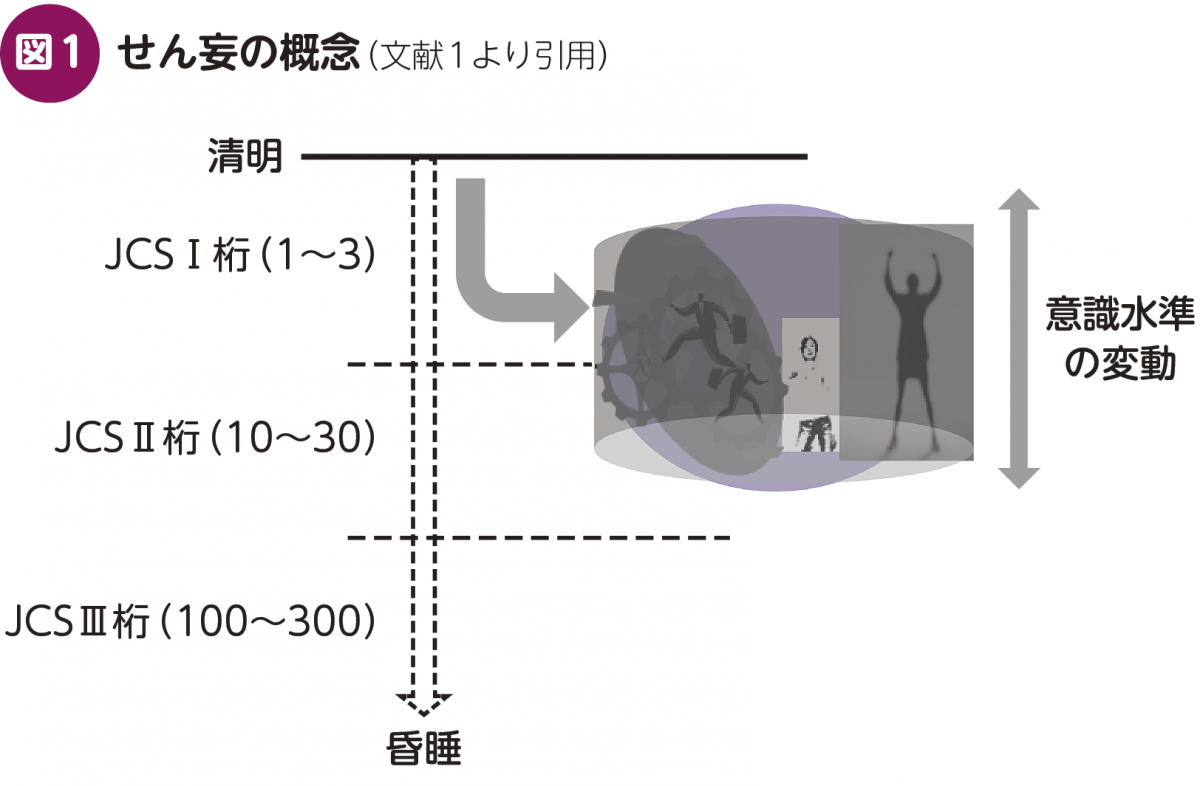
せん妄は,覚醒度の変化とその時間的な変動が本質的であり,それに伴い周囲の状況を認識できなくなったり,幻視・錯視といった視覚的な異常体験が優勢に出現したりする認知の変化を特徴とする。図1に示す通り1),軽度の意識の曇り(量的な低下)に質の変化(幻覚や精神運動性の異常)が重畳し,それが時間とともに変動する特殊な意識障害としてとらえると,全体像を理解しやすい。せん妄は,急性脳機能不全のひとつの表現型である。
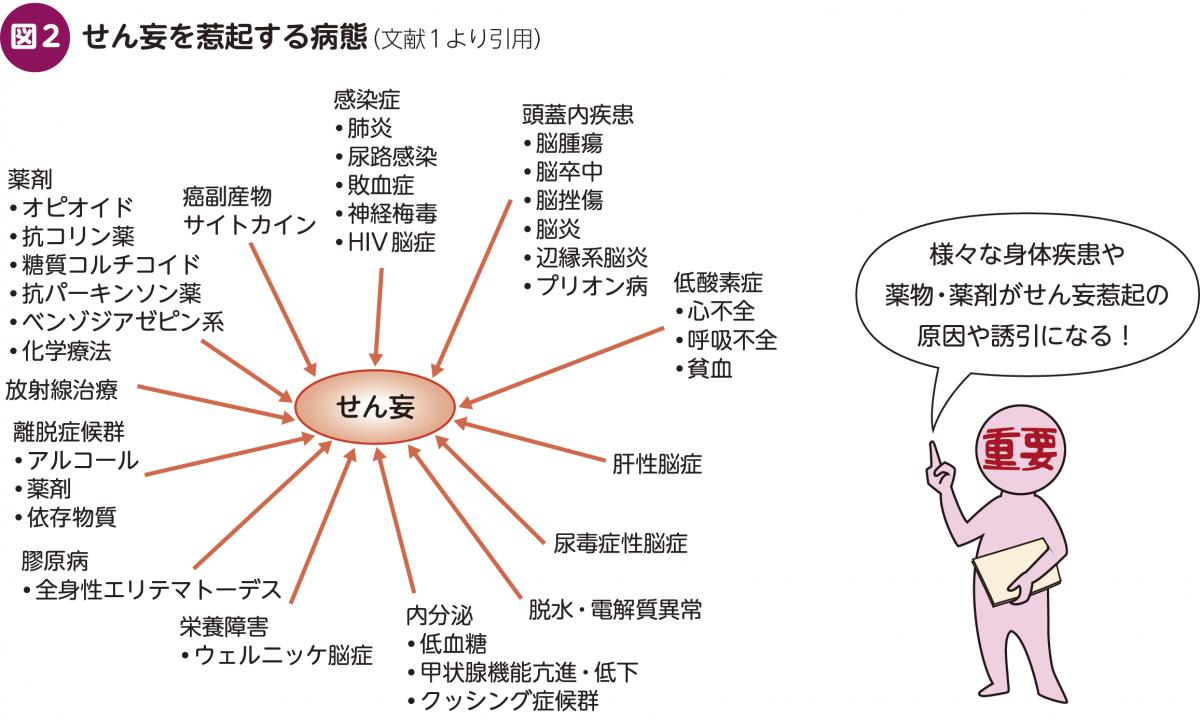
(2) せん妄を惹起する病態とその機序
図2に示した通り1),様々な身体疾患や薬物・薬剤がせん妄惹起の原因や誘因になる。それぞれの因子がどの程度のリスクになるかは,罹患率あるいは有病率といった指標が報告されているものもあるが,そうでないものも多い。また,報告されている罹患率や有病率は,集中治療室(ICU)なのか一般病棟なのか,内科系か外科系かなど,観察される状況によってかなりの幅がある。
せん妄の発症には,このような直接因子の衝撃の大小とともに,個々の患者の脆弱性,すなわち,せん妄の発症のしやすさを規定している準備因子の大小が大きく影響する。準備因子の代表例として,脳の加齢性変化が挙げられる。身体疾患で入院した患者に関する観察研究で,65歳未満ではせん妄発症が3%であったのに対して,65~74歳では14%,75歳以上では36%であったことが報告されている2)。高齢者が入院患者の大多数を占める昨今,この知見はベッドサイドでまさに実感を伴う数字である。また,老化の過程で進展する慢性虚血性変化も,重要な準備因子である。慢性虚血性変化が明らかな脳ほど,血液脳関門の透過性が亢進し3),そこから炎症や低酸素,薬物シグナルが中枢側に伝わりやすくなりミクログリアが活性化する。すると,ミクログリアからサイトカインなどが放出されて,アストロサイトや神経細胞にそのシグナルを伝えるカスケードが動きだす。一種の脳症で,急性脳機能不全の状態である。
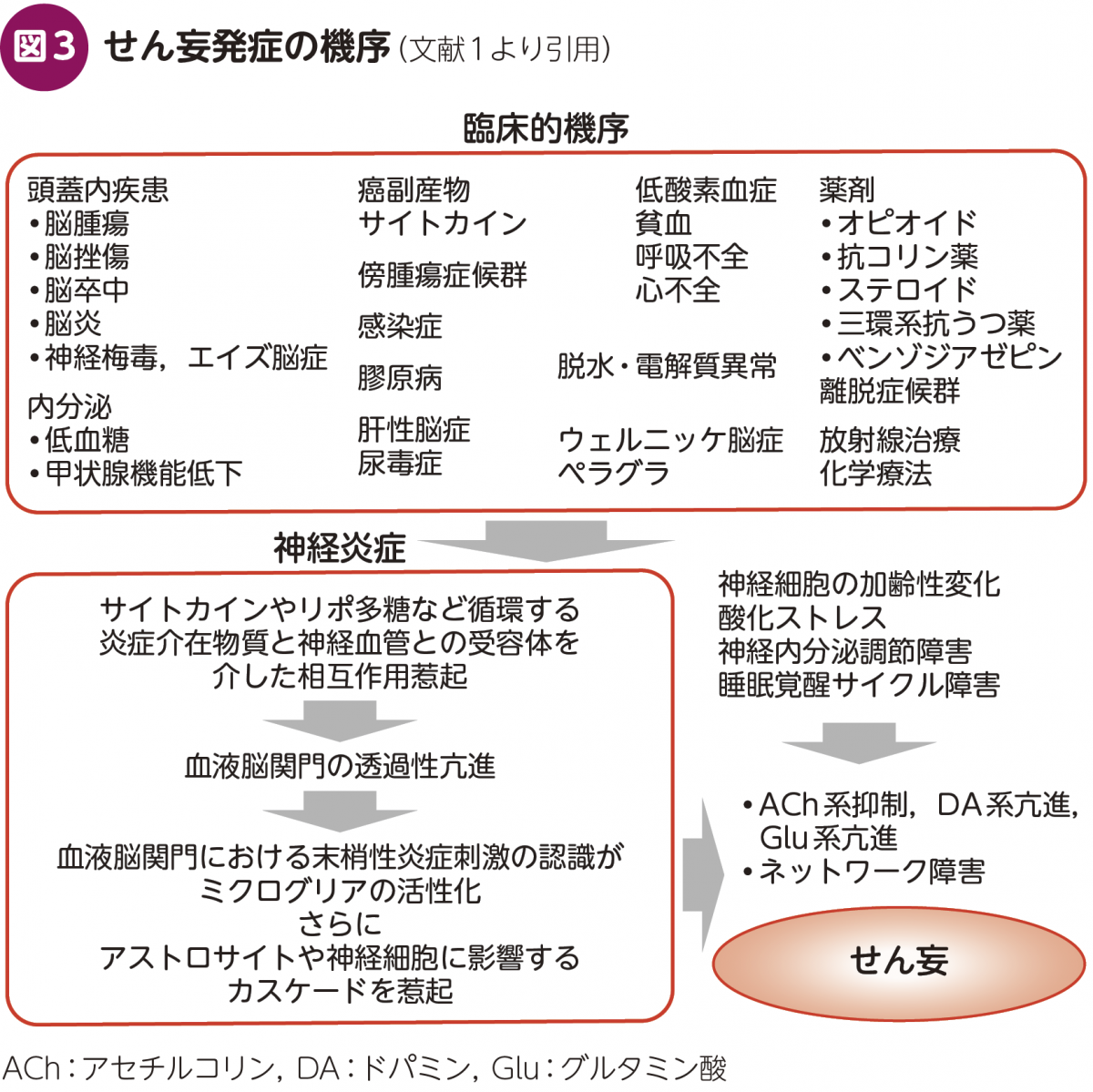
せん妄臨床で興味深いのは,原因や誘因となるのは様々な身体疾患や薬物・薬剤であるにもかかわらず,結果として共通するせん妄状態が惹起されることである。その理解には数多の神経科学的な知見・推論がまとめられており4)5),発症機序を簡略化すると図3のようになる1)。手術,炎症,外傷など様々な生体ストレス下では糖質コルチコイドが上昇するが,そのホメオスタシスが不調をきたす状況では,糖質コルチコイドの受容体が濃密に存在する海馬で,グルタミン酸遊離を促進することが示されている。実際,糖質コルチコイドの全身投与では,せん妄,うつ,躁,精神病症状,認知・記憶障害といった症状が60%に至る頻度で出現する。基礎研究でも,リポ多糖や細菌惹起の末梢炎症によるミクログリアの活性化が明らかにされており,敗血症惹起のせん妄の動物モデルとなっている6)。炎症は血液や脳脊髄液のグルコース低下を惹起し,行動変容につながることが示されている7)。低酸素機序については,術前のヘモグロビン低値や術中の酸素飽和度(SpO2)の低値と,術後の認知機能低下やせん妄との関連が示されている。また,低酸素状態ではグルタミン酸やドパミンの遊離が促進し,アセチルコリンの合成や遊離が抑制されることが示されている。抗コリン作用はミクログリアへのコリン作動性の抑制を解除するため,脳の免疫担当細胞であるミクログリアの暴走とも言える状態を惹起する8)。睡眠覚醒サイクル障害については,長期間の睡眠遮断で認知の障害やせん妄が惹起され,前炎症性サイトカインの増加,副交感神経系抑制と交感神経系亢進,夕方のコルチゾール値上昇などとの関連が示されている。ベッドサイドで観察していると,多くの場合,これらの機序が複合的に作用していることが推測される。
プレミアム会員向けコンテンツです
→ログインした状態で続きを読む