お知らせ
FOCUS:〈一病息災? それ,神経が生きてればの話です〉 糖尿病性神経障害の新たな診断基準案


◉糖尿病性多発神経障害(DPN)の診療は,自覚症状に対する対症療法に主眼が置かれ,本来の予防医学的見地からのアプローチは不十分である。
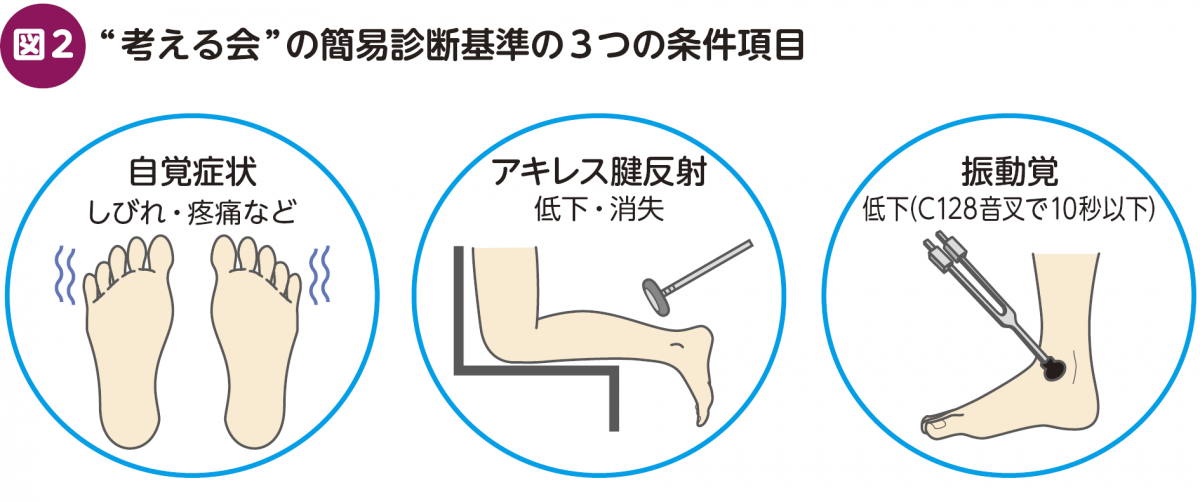
◉現在普及している糖尿病性神経障害を考える会の簡易診断基準は,自覚症状,アキレス腱反射および振動覚を用いた症候学的診断法であり,汎用性のある客観的・定量的な診断基準の整備が必要とされている。
◉本稿で紹介する新たな診断基準案は,従来の症候学的診断に加えて電気生理学的診断を追加しており,将来的な疾患克服につながることをめざしている。
◉電気生理学的診断を用いて,DPNを早期診断する臨床的意義を明確化することが今後の課題である。

❶ はじめに
糖尿病を患う人にとって,糖尿病の何が怖いのかを理解することがひと苦労である。著しい高血糖状態等を除けば,基本的には慢性に潜在的に経過する病気であり,病気による実害が生じるまでは無症状に経過する期間が長い。 “来年のことを言えば鬼が笑う”ではないが,その人の1回きりの人生で起こるかどうか,防げるかどうかも不明な有害事象のために,毎日コツコツと気をつけて治療に励むという行動は取りにくい。それでも,世界中で多くの患者が様々な制約を感じながら治療に取り組んでおり,その努力には脱帽せざるをえない。努力に報いるために筆者らいわゆる専門家は糖尿病の病態解明に取り組み,日常生活で制約が少なく,かつよりよい結果につながる治療の開発をめざしている。しかしながら残念なことに,本稿で採り上げる糖尿病性神経障害は,糖尿病の合併症の中では治療開発が周回遅れ,あるいはほぼ忘れられた存在となっている。まずは的確に診断できるようにする取り組みが必要な段階であり,本稿では診断に関する現状を中心に解説したい。
❷ 糖尿病性神経障害の分類と各種診断法
(1) 糖尿病性神経障害の疾患概念と分類
糖尿病性神経障害は広く受け入れられている定義はないが,一般的には“糖尿病に起因する末梢神経障害”という疾患概念で理解されている。ただし,この分野の研究者たちの多くは,糖尿病に起因するかどうかという点に違和感を抱いている。これまでの糖尿病性神経障害の病型分類には,糖尿病に起因する,真に“diabetic”な末梢神経障害と,非糖尿病患者にも認められるが,糖尿病患者により高頻度で認められる末梢神経障害が含まれてきた(表1)1)。
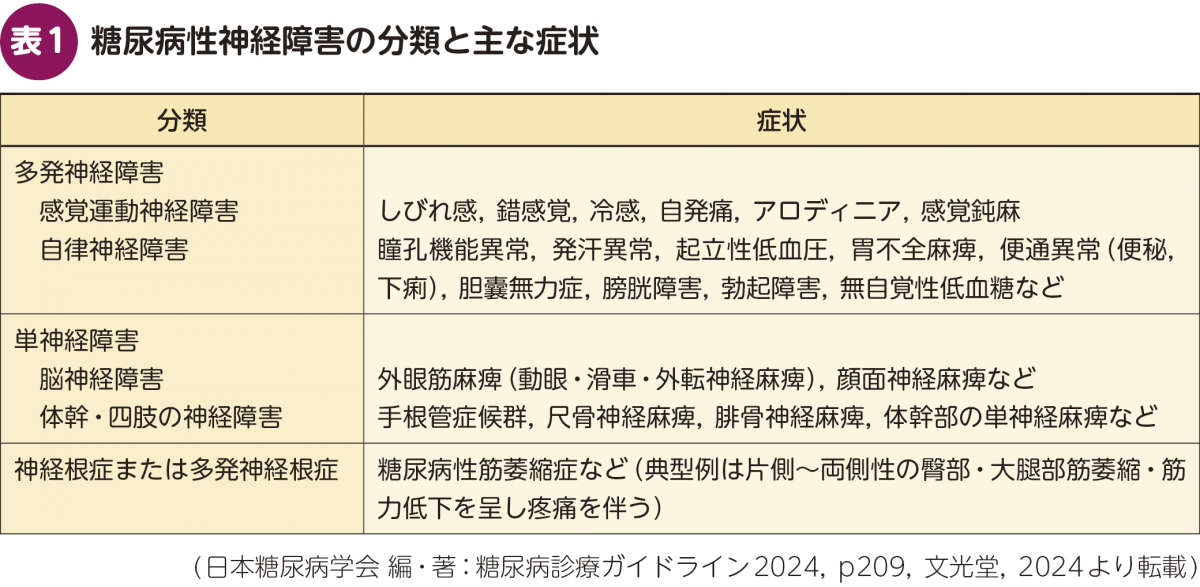
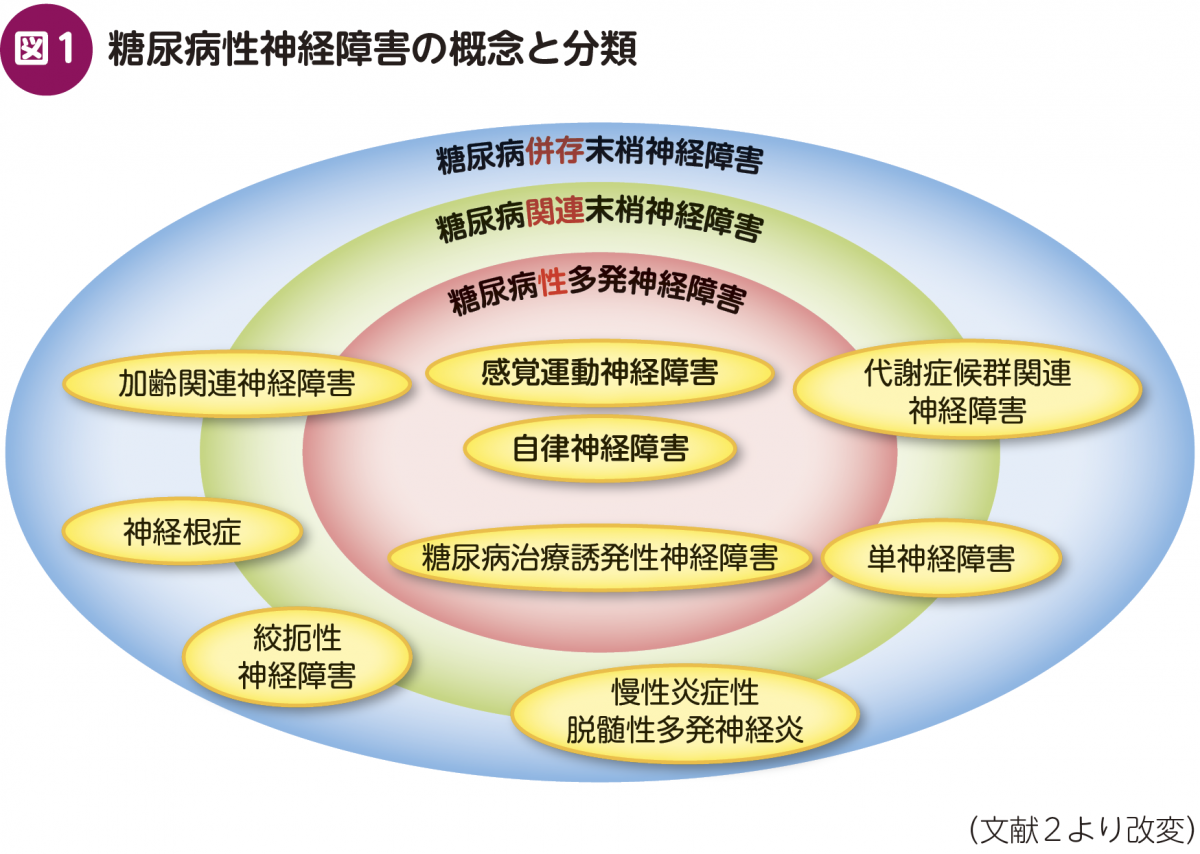
そこで筆者らは,この問いに対して深く向き合い,解決へと導く方法を探るために,まず手始めに糖尿病性神経障害を表現する用語を整理した(図1)2)。糖尿病患者に併存するが偶然か因果関係があるかが不明なものを含んだ疾患群を糖尿病併存末梢神経障害とし,糖尿病患者でより高頻度に認められるが糖尿病の病態に特異的ではないものを含んだ疾患群を糖尿病関連末梢神経障害とした。その上で,これらの疾患群の中核には糖尿病の病態によってのみ生じていることが確からしい疾患として,糖尿病性多発神経障害(diabetic polyneuropathy:DPN)を置いた。この整理に基づいた思考様式が単なる言葉遊びに終わらないよう,今後の国内外の研究活動を通じて糖尿病併存末梢神経障害の疾患一つひとつの病態が検証され,理解が深められることを期待している。
コラム❶ DPN以外の糖尿病性神経障害
DPN以外に,糖尿病の病態が発症の背景として,強く関連している可能性の高い神経障害を2つ紹介しておく。
【糖尿病治療誘発性神経障害(treatment-induced neuropathy of diabetes:TIND)】
治療後有痛性神経障害とも呼ばれていた病態である。高血糖状態を比較的長期間放置していた症例において,急速に血糖管理が改善した後,2カ月以内に,亜急性に神経障害性疼痛と自律神経障害が生じる。通常は,良好な血糖管理と,疼痛・立ちくらみなどに対する対症療法を継続することで1年以内に自然解消する。大径神経線維の機能を反映する神経伝導機能は,発症時に低下していても経過中に改善する症例もある。現時点で,このような臨床像を十全に説明できる病態仮説は確立されていない。
【代謝症候群関連神経障害】
一般に小径神経障害(small fiber neuropathy)と呼ばれる。この20年ほどで小径神経線維を評価できる定量的検査がいくつか確立されており,その過程で前糖尿病状態や代謝症候群の患者においても,小径神経線維の異常が証明されてきた。2017年に発表された米国糖尿病学会のposition statementには,小径神経障害を主たる臨床像とする遠位対称性多発神経障害が一分類名として提案されており,脂質代謝異常や内臓脂肪蓄積が病態の主要部分を説明できると想定されている。ただし,大径神経線維の機能を反映する神経伝導機能は9割前後の糖尿病患者で異常を認めることから,糖尿病患者において純粋な小径神経障害型のDPNは少なく,DPNの発症・進展との関係性は解明途上である。
(2) DPNの病態
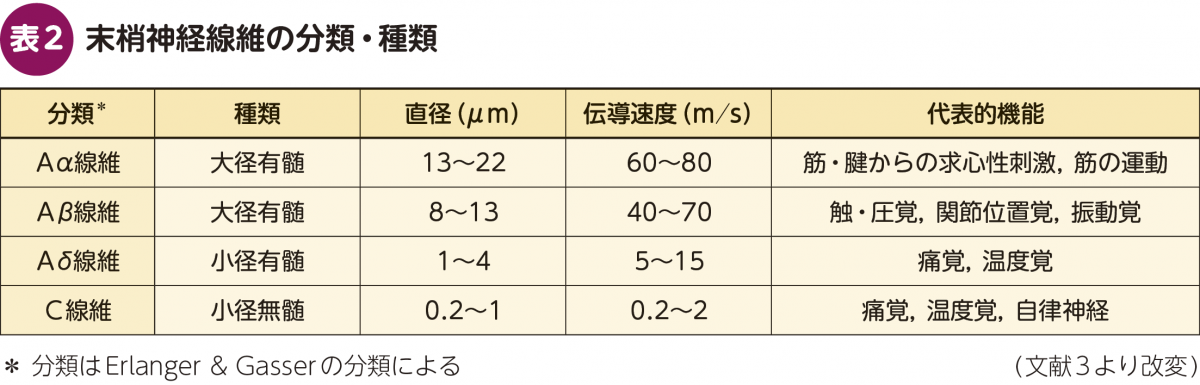
歴史的には,DPNは神経生検を用いた病理学的所見によって病態の基盤が確立された。末梢神経系は,感覚運動神経系(体性神経系)と自律神経系に大別されるが,いずれの神経系もDPNで障害される。神経線維は,太さによってそれぞれの機能は異なるが,大まかにわけると最も細いC線維は自律神経系と感覚神経系が占め,それよりやや太いAδ・Aβ線維が感覚神経系であり,最も太いAα線維が運動神経系となる(表2)3)。DPNでは,これらのいずれの太さの神経線維も障害を受ける。この障害は,感覚運動神経系では下肢遠位に行くほど高度である。自律神経系における病理学的変化は限られた知見しか存在せず,感覚運動神経系に認められるような遠位優位の変性が主体であるかは不明である。
障害の様式は軸索変性が主体であるが,シュワン細胞の変性による脱髄病変も一部混在しており,DPNの病態形成に関わる因子が単一ではない可能性を示唆している。下肢遠位での病態は,びまん性軸索変性が主体であるが,大腿レベルでは局所性軸索変性が認められ,虚血の要素が関与していることが示唆されている。ただし,大腿レベルまで含めた神経生検の実施症例は限られており,多くは虚血性下肢病変を合併した下肢切断例,あるいは剖検例での知見をもとにしている。これらの症例における病理学的変化が,どの程度一般化できるかは不明である。したがって,基本的にDPNの病態は複数の要素で構成されると推察されるものの,どの要素が重要であるかについては個体差が大きいと理解すべき学術段階である。
(3) DPNの診断法の選択と罹病率
国内外の多くの総説・論文などでは,DPNは糖尿病患者の約半数に認められるとされる。しかしながら,診断法によって罹病率は約2~9割強まで幅があり(表3),罹病率を以てしてDPNの重要性を語ることは困難である。このように疫学上基本的な項目である罹病率ですら報告によって大きく異なることは,この疾患を理解する上で大きな障壁となっており,解決が望まれている。
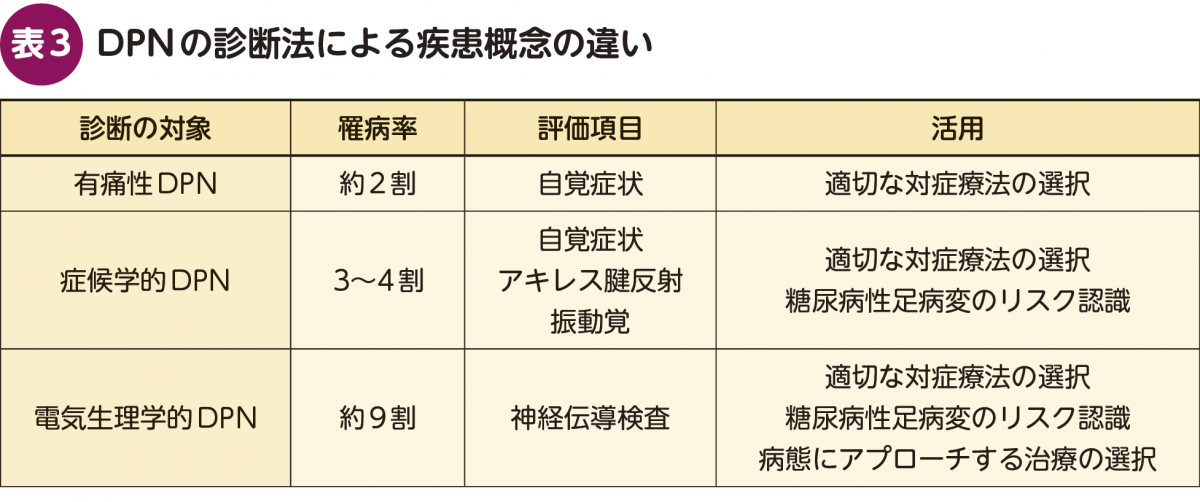
現状では医療者側の様々な要請・目的によってDPNの診断法が選択されている。DPNを患者の主観的な症状(痛み,しびれ,異常感覚など)に基づいて診断する,いわゆる有痛性DPNを対象とした場合は,約2割の罹病率となる。ここにさらに,アキレス腱反射・10gモノフィラメントによる触覚検査・音叉による振動覚などの理学所見を加えると,いわゆる症候学的DPNを診断でき,その場合は3~4割の罹病率となる。一方で,これらの症候学的項目とは独立して,神経伝導検査によって電気生理学的DPNを診断すると,軽微な異常所見まで含め罹病率は一気に約9割に達する4)。特に,脛骨神経のF波最小潜時については,2型糖尿病と診断された時点でほぼ100%の患者で延長を認めるという既報が複数存在し,F波潜時というほぼ下肢全長の神経伝導機能を評価できる項目を用いれば,運動神経伝導速度の低下を明確化できることがわかる。
根本的には,DPNは全身の糖代謝異常に付随する末梢神経系の異常であることをふまえると,有痛性あるいは症候学的DPNを疾患の基本概念とすることについて医学上の合目的性はない。有痛性DPNは患者のQOLを改善する目的で積極的に診断する必要があり,症候学的DPNは糖尿病性足病変(足壊疽,皮膚潰瘍など)を予防するための啓発目的で診断する必要がある。しかしながら,末梢神経系の変性の発症・進展を予防あるいは治癒させるためには,糖尿病の発症時より付随する末梢神経機能異常を的確に診断し,その病態を明らかにすることが疾患克服に向けた取り組みの中で欠かすことのできない重要な第一歩となる。
(4) DPNの診断法の変遷と課題
DPNにおいては,疾患の進行,すなわち軸索変性などの末梢神経変性の進行とともに神経線維数は減少する。この病理学的変化の度合いと,神経伝導検査による神経機能低下の程度が比較的良好に相関することが示され,神経伝導検査が侵襲的な神経生検による診断を代替するゴールドスタンダードとして認識されるようになった。しかしながら,神経伝導検査は高額な検査機器と習熟した技術者,そして結果を解釈できる専門家が必要なことから,実施できる医療機関は限られている。そのため,神経伝導検査を罹病者数の多い糖尿病患者にスクリーニング的に広く実施することは現実的ではなく,過去数十年にわたって国内外で様々な簡易的な症候学的診断法が提唱されてきた。そうした活動を通じて,モノフィラメントによる触覚検査や音叉を使った簡易的な振動覚検査が糖尿病性足病変のハイリスク患者の抽出に有用であることが示され,実臨床に活用されてきた。
日本では,糖尿病性神経障害を考える会が1998年に提唱した「糖尿病性多発神経障害の簡易診断基準」が糖尿病性神経障害の症候学的診断法として広く用いられており,本疾患を啓発する点でも多大な貢献をしてきた(表4)5)。診断には自覚症状とアキレス腱反射,振動覚を用いており,特別な検査機器などを用いなくても日常的に診断できることが特徴である(図2)。この簡易診断基準を通じて,糖尿病性神経障害には特異的な症状や所見は存在せず,自覚症状と神経学的身体所見から総合的に診断する必要があるということが,国内の医療者・患者に広く伝わってきたと考えられる。また,これらの症候学的異常所見が,下肢の遠位を中心として左右対称性に発症・進行するという特徴も多くの医療者の常識となるところまで普及させてきた。一方で残念ながら,この簡易診断基準を通じて新たな治療薬・治療法を開発するという気運は広がらず,症候学的診断基準を疾患修飾的治療法の開発につなげることの限界が示唆されている。

海外においては,上述の症候学的診断法に類似する基準がいくつか提案されてきたが,近年では「Toronto Diabetic Neuropathy Expert Group」による診断の考え方,いわゆる,“トロントコンセンサス”が広く認識されている。トロントコンセンサスでは,臨床においては広く症候学的な評価を行い,probableあるいはpossibleな糖尿病性神経障害を診断することが推奨されている。一方で,学術的な確定診断のためには,神経伝導機能異常を証明する必要性が明記されており,神経変性疾患としての病態を正しく診断するためには,電気生理学的診断が必須であるという考え方が改めて明示された。
以上の現状をふまえ,疾患修飾的治療法を開発するためには,電気生理学的診断による正確な診断が前提になると考え,筆者らは新たな診断基準の策定を進めてきた。
コラム❷ アキレス腱反射の実施・判定法
【道具】
アキレス腱は太く,反射を誘発するためには十分な強度の刺激を与える必要がある。よく見かけるTaylor型打腱器では強度不足であり,ヘッドが円形で重いQueen Square型やBabinski型の打腱器が推奨される(図3)。
【姿勢】
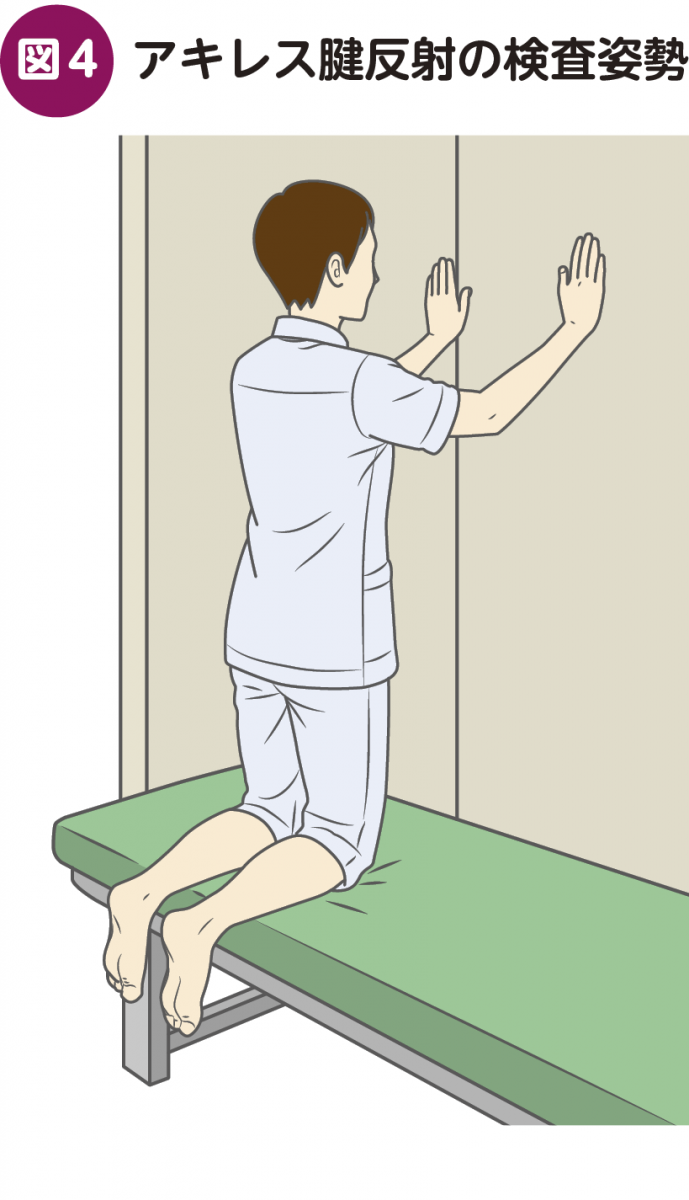
医学部などでは,坐位や仰臥位での評価の仕方が教えられているが,習熟者でなければ安定して反射を誘発できない。膝立ちで背筋を伸ばして両手を壁につく,あるいは椅子の背をつかむ姿勢のほうが,アキレス腱に安定した刺激を与えられる。脳神経内科医などの専門家以外の医療者が実施する際には,この膝立位が推奨される(図4)。
【判定法】
正常:打腱器で叩いたタイミングで足が動く,あるいは足を動かそうとする筋緊張が足を把持した手に伝わる。
低下:増強法*を用いて初めて前項(正常)の反応が確認できる。
消失:増強法を用いても反応が確認できない。
*増強法:背筋と肘をぴんと伸ばすよう指示した上で,「1,2,3の合図で歯を食いしばって下さい」と声をかけ,歯を食いしばった瞬間にアキレス腱を叩く
【注意事項】
1. 叩打する前に,打腱器を持っていない側の手で患者の足を把持し,前後に優しく動かすことで足関節の緊張が取れているかを確認する。足関節の緊張があるときは力を抜くように声をかける。
2. 叩打する際は手首のスナップを利かせる。
3. 叩打する部位がずれていることがあるので,叩打部を少し上下にずらしながら何回かリズミカルに叩いてみて,反射が出ないか確認する。

コラム❸ 振動覚の評価法
【道具】
一般的なC128Hz音叉を用いる。時間の計測器具(ストップウォッチなど)も用意する。
【判定法】
掌に打ちつけて強く振動させたC128Hz音叉を足関節の内踝に当て,振動を感知できる時間が10秒より長ければ正常,10秒以下であれば低下とする。
【注意事項】
1. 事前に,音叉の振動を患者の胸骨や手背に当て,振動を体験させる。この際に,「振動を感じなくなったら“はい”と言って下さいね」と伝え,振動する音叉を胸骨などに当て,しばらくしてから音叉を持たないほうの手で強制的に振動を止め,速やかに“はい”と答えられるかを確認しておく。応答が速やかでない場合はできるようになるまで何回か訓練する。症例によっては,振動していない音叉を当てて振動の有無を尋ねることも有用である。
2. 計測する時間は音叉に振動を与えた瞬間からであり,音叉を内踝に当ててからではない。
プレミアム会員向けコンテンツです
→ログインした状態で続きを読む
















































