
しらき きみやす:1977年阪大卒。2013年富山大学医学部学科長,2019年4月から現職。専門は臨床ウイルス学。新型コロナウイルス感染症の治療薬の候補に挙がっている抗インフルエンザウイルス薬ファビピラビル(商品名:アビガン)を開発
No.5004 緊急寄稿(1)新型コロナウイルス感染症(COVID-19)のウイルス学的特徴と感染様式の考察
No.5005 緊急寄稿(2)COVID-19治療候補薬アビガンの特徴
No.5036 緊急寄稿(4)新型コロナウイルス感染症(COVID-19)に対するアビガン承認に向けて
1. はじめに
前稿(No.5005),前々稿(No.5004)で,新型コロナウイルスのウイルス学的特徴を推測し,抗ウイルス薬ファビピラビル(商品名:アビガン)の開発過程とCOVID-19肺炎への治療効果について紹介した。本稿では,ウイルス感染症と細菌感染症の違いや種々の抗ウイルス薬の作用の特徴などについて解説する。
2. ウイルス感染症の特徴(表1)

ウイルス感染症は,ウイルスの種類によりそれぞれ特徴がある。ここでは,インフルエンザ型と水痘型に分けて紹介する。
インフルエンザはウイルスが上気道粘膜に感染して,細胞内にウイルスRNAを産生する。このような異物RNAを細胞内のToll様受容体が認識して,異物に対する自然免疫として種々のサイトカインにより炎症や発熱を誘導し1),既存免疫が応答する前に発熱等で発症する。ヒトへの実験的感染では18時間で発熱するが,日常の感染では1~2日の潜伏期間がある。水痘は,潜伏期2週間で皮膚や内臓で増えたウイルスに対する免疫が立ち上がり,感染細胞等に対する免疫応答により,丘疹,紅斑,水疱,膿疱,痂皮と症状が推移する。
COVID-19は潜伏期間が1~14日〔中央値は5.1日(95%CI;4.5~5.8)〕で,対象患者の97.5%が感染から11.5日(8.2~15.6)以内に発症すると推計される2)。COVID-19による肺炎は,新型コロナウイルスがインフルエンザウイルスと同じRNAウイルスであることと,発症後に増強される点や潜伏期間の長さを考えると,上記のサイトカインによる炎症(インフルエンザ型)と感染細胞等に対する免疫応答による炎症(水痘型)が重なり,肺炎を起こしていると考えられる。したがって,COVID-19肺炎は,ウイルスの増殖範囲が限られた初期に治療を開始して,重症化を防ぐことが望ましいと思う。
3. ウイルス感染症と細菌感染症の治療効果の違い(表1)
細菌感染は,細菌が通常20分〜1時間で増殖し,それと戦う炎症が生じる。したがって1回の抗菌薬投与で菌が死滅し,炎症は収まり始めるため,抗菌薬の即効性を実感できる。
ウイルス感染では,SARSやインフルエンザは感染6時間,水痘は約14時間で新しいウイルスが放出され増加していく。ここに抗ウイルス薬が作用すると新たな感染細胞はできなくなるが,既感染細胞ではウイルスの増殖は続き,抗原は作られ続ける。オセルタミビル(商品名:タミフル)に比べ、アビガンで処理したインフルエンザ感染マクロファージ様細胞やインフルエンザ感染マウスでは,TNF-α産生を低下させるが,他のサイトカインの変動は見られない3)。TNF-αは,最初に誘導され一番早く消失するため,RNA合成阻害薬であるアビガンでさえ,感染細胞や感染動物でのサイトカイン産生抑制は限られる。
ウイルス感染症と細菌感染症の治療効果の違いの具体例として,細菌感染である伝染性膿痂疹(とびひ)と,ウイルス感染である水痘や帯状疱疹を比較してみる。
朝,とびひに対して抗菌薬で治療を開始すると,夕方か翌日には皮膚症状の軽減が実感できる。広範囲にとびひが広がっても抗菌薬は1日で有効性を示す。しかし,水痘や帯状疱疹では,皮疹出現時に抗ヘルペス薬を投与すると新たな感染細胞は形成されないが,発赤や皮疹は消失しない。ウイルスに対する免疫応答の成熟で見かけ上の炎症が強くなるためで,皮疹が増悪することもある。そして皮疹の改善には数日を要する。水痘では,水疱にまで進んでから抗ウイルス薬を投与しても治癒を促進しない。水疱以降の症状は免疫応答による回復過程なので,抗ウイルス薬の効果は期待しにくい。
肺炎治療についても違いがある。細菌による気管支肺炎では抗菌薬で細菌が死滅すれば炎症は収まるし,炎症は気管支,細気管支から肺胞内の管腔に生じるので,炎症後の肺実質の線維化や瘢痕化等の後遺症は起こしにくい。
ウイルス性肺炎では抗ウイルス薬によって新規感染細胞の形成を阻止しても,既感染細胞からはRNAによるサイトカインを放出し続けるので,その細胞の周囲の炎症は続く。さらに,その感染細胞に対する免疫応答は成熟し強くなる。COVID-19肺炎は,インフルエンザ型と水痘型の複合的炎症による間質性肺炎と考えられるので,SARS肺炎の回復後にもみられたような線維化や瘢痕化等の後遺症を生じるものと思われる。SARS肺炎は4週目には55%に早期の線維化の兆候を認めるなど,肺の画像上に変化を残している4)5)。ウイルス性肺炎では,細菌性肺炎の治療と同じように考えないことが重要と思う。
なお,中国・深圳の病院で実施した臨床試験では,アビガン群ではウイルス消失までに4日かかり(対照群のカレトラは11日),胸部CT所見の軽症化は9日の時点ではカレトラ群と変わらないが,投与後14日目の胸部CT所見の改善率は91.43%であり,カレトラ群の62.22%と比べて有意に改善し,カレトラ群ではまだ20%に悪化を認めていた。このように,ウイルスの消失に比べ,炎症の回復まで時間がかかっている6)。
以上から,COVID-19肺炎は,約6時間で既感染細胞から新たな感染細胞を作り,1日でウイルス増殖の4サイクル分のスピードで感染が肺内で広がると考えられる。肺炎の予後は予測できないので,肺炎を見つけたら発症後6日までにアビガン治療を開始して,早期のウイルス消失と,重症化や後遺症を防ぐことを考慮していただきたい。
4. PCRと感染性ウイルス
感染性ウイルスの割合は1/100~1000のウイルス粒子からなる。したがって,ウイルスの検出に用いられるPCR検査は,分離による感染性ウイルスの検出より約1000倍感度は高いので,診断の価値は高い。現在のPCR法は,定量(リアルタイム)PCRなので,陽性か陰性かだけではなく,ウイルスゲノム数を直接測定できる。
COVID-19は,咽頭のウイルスは発症とともに検出される。ウイルス量は10日がピークで,12~15日で減少する。鼻咽頭には症候性患者と無症状感染者も同等のウイルス負荷があるため,無症状感染者からの感染の可能性が示唆されている7)。呼吸器症状の有無にかかわらず,ゲノム数が多ければ,病勢の評価,周囲への感染リスクの評価等に使用できると思われる。すでに,数千件を超えるPCR検査の結果があるはずなので,回復した患者はゲノム量が少ないなどの,PCR法による病態分類が示されることを期待したい。
5. 抗インフルエンザ薬の作用機序と耐性出現の可能性
アビガンは抗ウイルス薬の中でも例外的に耐性ウイルスが生じず,最初から最後の患者まで同じ有効性を維持できる。そこで,アビガン以外の抗インフルエンザ薬は薬剤耐性ができるのに,なぜアビガンは耐性ができないかを少し難解な内容となるが解説したい。
図1に現在使用されている抗インフルエンザ薬の作用部位を示す8)。タミフルとバロキサビル マルボキシル(商品名:ゾフルーザ)は,ウイルスRNA合成は許すが,その後のステップで,ウイルスの感染細胞からの広がりを阻害して,抗インフルエンザ活性を示す。
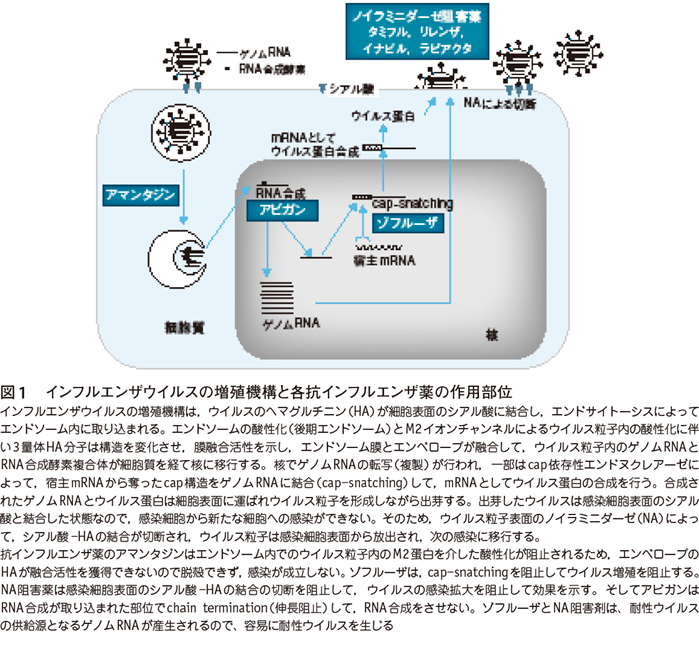
インフルエンザウイルスは約10kb(1万塩基)からなり,ウイルス感染細胞の培養上清には感染性粒子が108/mL程度産生される。遺伝子複製中に変異は1/104の頻度で生じるため,細胞内で産生されたウイルスの遺伝子は,どの塩基も1/104の頻度で変異しており,薬剤耐性ウイルスの供給源となる。そのため,小児のタミフルやゾフルーザによる治療終了時には約10%に耐性ウイルスが見られる。このようにウイルスRNA合成後に作用する薬剤は,作用機序的に耐性株の出現は避けがたい。
アビガンは,ウイルスRNA合成を阻止することと,RNA依存性RNAポリメラーゼ(Rd Rp)の共通性の高い部位に作用するため,耐性ウイルスを生じない。アビガンのインフルエンザの臨床試験では,アビガン投与前後の57ペアのウイルスの感受性に変化はなく,耐性ウイルスは分離されなかった9)。インフルエンザウイルスとポリオウイルスを1カ月間アビガンの存在下で培養しても,耐性ウイルスは生じなかった8)10)11)。遺伝子組換え技術により単独で増殖できる耐性ウイルスが報告されたが,ウイルス全体を置き換えるような増殖能を持たない12)。したがってアビガンは,タミフルやゾフルーザなどで見られるように,治療中にアビガン耐性ウイルスに置き換えられるような問題は発生しないと考えられる。このように、アビガンの特性は致死性重症感染症に対する優れた効果だけでなく、耐性ウイルスができない点にもある。
6. その他の薬剤耐性と病原性
細菌感染症における薬剤耐性は,ペニシリンやテトラサイクリンのようにプラスミドによる耐性とキノロンのようなゲノム遺伝子の耐性がある。プラスミドによる耐性は宿主ゲノムに変化はないので細菌の持つ増殖性や病原性に変化はない。宿主遺伝子変異による耐性は多少増殖性に影響が出るかもしれないが,あまり病原性の低下は認めない。
抗ウイルス薬には,アビガン,アシクロビル,核酸系抗HIV薬のように遺伝子複製を阻害する薬剤と,タミフル,ゾフルーザ,HIVプロテアーゼ阻害薬などのように遺伝子複製後にウイルスの成熟や感染の拡散を阻害する薬剤がある。前者は,耐性ウイルスの供給源となる遺伝子が複製できないので,後者に比べ耐性ウイルスはできにくい。後者はウイルス感染後細胞内にウイルス遺伝子ができてからの阻害なので,遺伝子複製中に1/104〜6の頻度で変異を生じる中で耐性遺伝子ができる。したがって,前者に比べ短時間で薬剤耐性ウイルスに置き換わりやすい。
薬剤耐性ウイルスは一般的に増殖に関する遺伝子に変異があるので増殖は損なわれている。そのため,増殖スピードは遅く多少潜伏期間は延びるが,病原性は変わらない。2009年の新型インフルエンザは,タミフル耐性インフルエンザが野生株を駆逐しながら世界的流行を起こしたように,耐性株であっても増殖能を有しているし,野生株同様の病原性も有している。
以上のように,遺伝子複製後に作用する抗ウイルス薬はその宿命として耐性を生じやすいため,ウイルスの増殖期間が長い場合には,HIV感染症治療と同様に,遺伝子複製の阻害薬と併用して,耐性出現を最大限抑制することが必要である。COVID-19においては,単独使用は治験で有効性を確認する以外では慎むべきと思う。
7. アビガン治療について
1)有効性と副作用
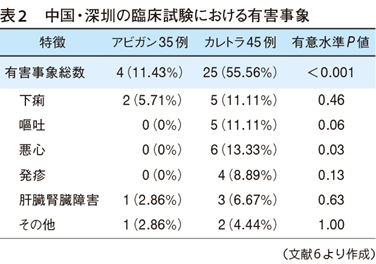
前稿(No.5005)で中国の2つの臨床試験(武漢,深圳)の結果から,アビガンのCOVID-19肺炎に対する有効性について述べた。水痘や帯状疱疹の治療開始は水疱形成まで待たないように,COVID-19も肺炎が起きれば早期に治療を開始すべきと思う。しかし,動物実験では妊孕性に問題があるので,妊婦は禁忌である。動物実験では精子形成の問題もあったがヒトでは認められず,承認前の約500名の臨床試験では肝機能や腎機能の障害等も確認されていないが,有意に尿酸値の上昇を認め(添付文書に記載),武漢の臨床試験でも,アビガン群は尿酸値が有意に上昇した〔13.8%(16/116):2.5%(3/120)〕13)。一方,アビガンとカレトラを比較した深圳の臨床試験では,カレトラが有意に有害事象を認めた(P<0.0001)(表2)6)。有効性と副作用のバランスを考慮してアビガンの投与を検討していただきたい。
2)エボラ出血熱から致死性感染症治療薬の臨床試験の難しさを学ぶ
アビガンが日本で抗インフルエンザ薬として承認された2014年,西アフリカでは死亡率約30%のエボラ出血熱が流行していた。アビガンは広い範囲のRNAウイルス感染症に有効であることから,その有効性が発揮される機会となった。
英国では,エボラウイルス感染マウスに対して,感染と同時にアビガンを予防投与した結果,全マウスが生存することを報告した14)。ドイツでは,感染6日目からの治療は全マウスを生存させるが,8日目からでは5匹中4匹が死亡し,早期投与の重要性を示した15)。
2014年8月に世界保健機関(WHO)専門家委員会は,エボラ出血熱に開発段階の治療薬やワクチンを使用することは倫理的に問題ないとする認識を示した。標準的治療薬がないなか,動物実験の結果からアビガンへの期待が高まった。
そして,11月からフランスはギニアで,中国はシオラレオネでアビガン(中国は独自のファビピラビル)を投与する臨床試験を開始した。薬剤の臨床評価はプラセボと実薬のランダム化比較試験(RCT)が標準であるが,約30%が死亡する致死性感染症のエボラ出血熱ではプラセボの設定が倫理的に難しい。アビガンは動物実験では命を救っていることから,結局,全員が治療対象になった。詳細は省くが,副作用の懸念から,女性や子供を対象としないことも予定されていたが,家族で治療に来た場合に命の選別をすることは無理であったようだ。また,発症早期のような病状を訴える患者への問診とPCR検査のウイルス量の関係が相関せず,問診に基づく発症時期の解析も困難であったようだ。
両試験ではプラセボの代わりに,投薬準備が整うまでの患者を歴史的対照・無治療群として,生存率等を比較した。その結果,ギニアでは死者を減少させたが有意ではなく(P=0.052),シオラレオネでは有意に死亡率を下げた16)17)。
この経験は,致死性感染症における薬剤評価の倫理的問題,臨床試験の難しさを如実に示している。アビガンはエボラ出血熱の治療に参加した医療関係者の針刺し等の暴露後予防に使用され,感染が防がれている18)。HIVの針刺し事故に関しては,RCTをしなくても有効性の積み重ねにより,現在では予防投与がガイドラインに記載されているように,致死性感染症はRCTができなくても,有効性を示す結果の蓄積が重要であると思われる。
8. おわりに
中国では,COVID-19肺炎に対するアビガン投与が診療ガイドラインに組み込まれる予定だ。中国の臨床試験の結果から,現時点で,アビガンより有効な抗ウイルス薬は幻想でないかと思う。アビガンは日本発の医薬品であるが,その薬剤の評価は国内からではなく,インフルエンザは米国から,エボラ出血熱は欧州とアフリカから,COVID-19は中国からもたらされた。これまでに述べてきたような,ウイルス感染症と抗ウイルス薬の作用の特徴を理解して,今後の診療に役立てていただけることを願う。
令和を迎える際の日本医事新報の特集(2019年5月4日号「医療の近未来予想図」)で私はアビガンについて,「『アビガンがあって良かった』と評価されるような新型インフルエンザ・パンデミックが発生しないことを期待したい」と書いた。実際に,COVID-19パンデミックで「切り札・アビガン」を使うことになった今,複雑な気持ちである。
【文献】
1) Kurokawa M, et al:J Med Virol. 1996;50(2):152-8.
2) Lauer SA, et al:Ann Intern Med. 2020 Mar 10.
3) Tanaka T, et al:Acta Virol. 2017;61(1):48-55.
4) Ooi GC, et al:Respirology. 2003;8(Supp l):S15-9.
5) Lau AC, et al:Respirology. 2004;9(2):173-83.
6) Cai Q, et al:Engineering. 2020 Mar 18.
7) Zou L, et al:N Engl J Med. 2020;382(12):1177-9.
8) Shiraki K, et al: Pharmacol Ther. 2020:107512.
9) Takashita E, et al:Antiviral Res. 2016;132:170-7.
10) Daikoku T, et al:J Microbiol Immunol Infect. 2018;51(5):581-6.
11) Daikoku T, et al:J Pharmacol Sci. 2014;126(3):281-4.
12) Goldhill DH, et al:Proc Natl Acad Sci U S A. 2018;115(45):11613-8.
13) Chen C, et al:medRxi V. 2020 Mar 17.
14) Smither SJ, et al:Antiviral Res. 2014;104:153-5.
15) Oestereich L, et al:Antiviral Res. 2014;105:17-21.
16) Bai CQ, et al:Clin Infect Dis. 2016;63(10):1288-94.
17) Sissoko D, et al:Plos Med. 2016;13(3):e1001967.
18) Jacobs M, et al:Lancet Infect Dis. 2015;15(11):1300-4.





