
❶ 左室の駆出率が保たれていても心不全になる
「2025年改訂版心不全診療ガイドライン」(日本循環器学会/日本心不全学会合同ガイドライン)において,心不全は「心臓の構造・機能的な異常により,うっ血や心内圧上昇,およびあるいは心拍出量低下や組織低灌流をきたし,呼吸困難,浮腫,倦怠感などの症状や運動耐容能低下を呈する症候群」と定義されている。心不全は,心エコー図検査などで測定される左室駆出率(left ventricular ejection fraction:LVEF)に基づいて分類される。具体的には,LVEFの低下した心不全(heart failure with reduced ejection fraction:HFrEF),LVEFの軽度低下した心不全(heart failure with mildly-reduced ejection fraction:HFmrEF),LVEFの保たれた心不全(heart failure with preserved ejection fraction:HFpEF),LVEFの改善した心不全(heart failure with improved ejection fraction:HFimpEF)にわけられている(表1)1)。
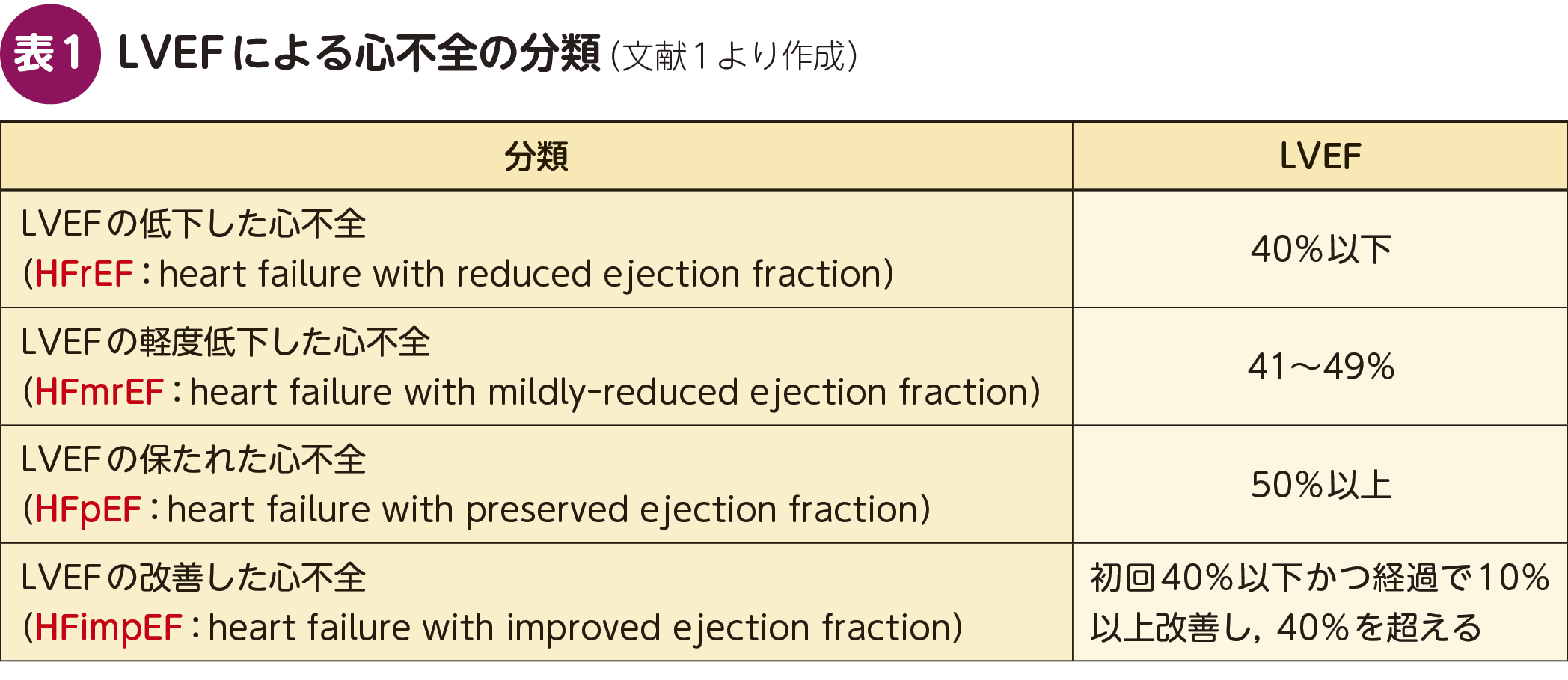
一般的に,LVEFが低下すれば心不全を発症するというイメージを持たれることが多いが,実際にはLVEFが保たれていても,心不全は生じうる。これは,心不全が単に駆出率の低下のみで説明される病態ではなく,心機能のほかの側面,すなわち拡張能低下,心房機能低下,体・肺血管との相互作用,右心機能低下,さらには全身性炎症や代謝異常といった要因が複雑に心不全の病態形成に関与しているためである(図1)2)。
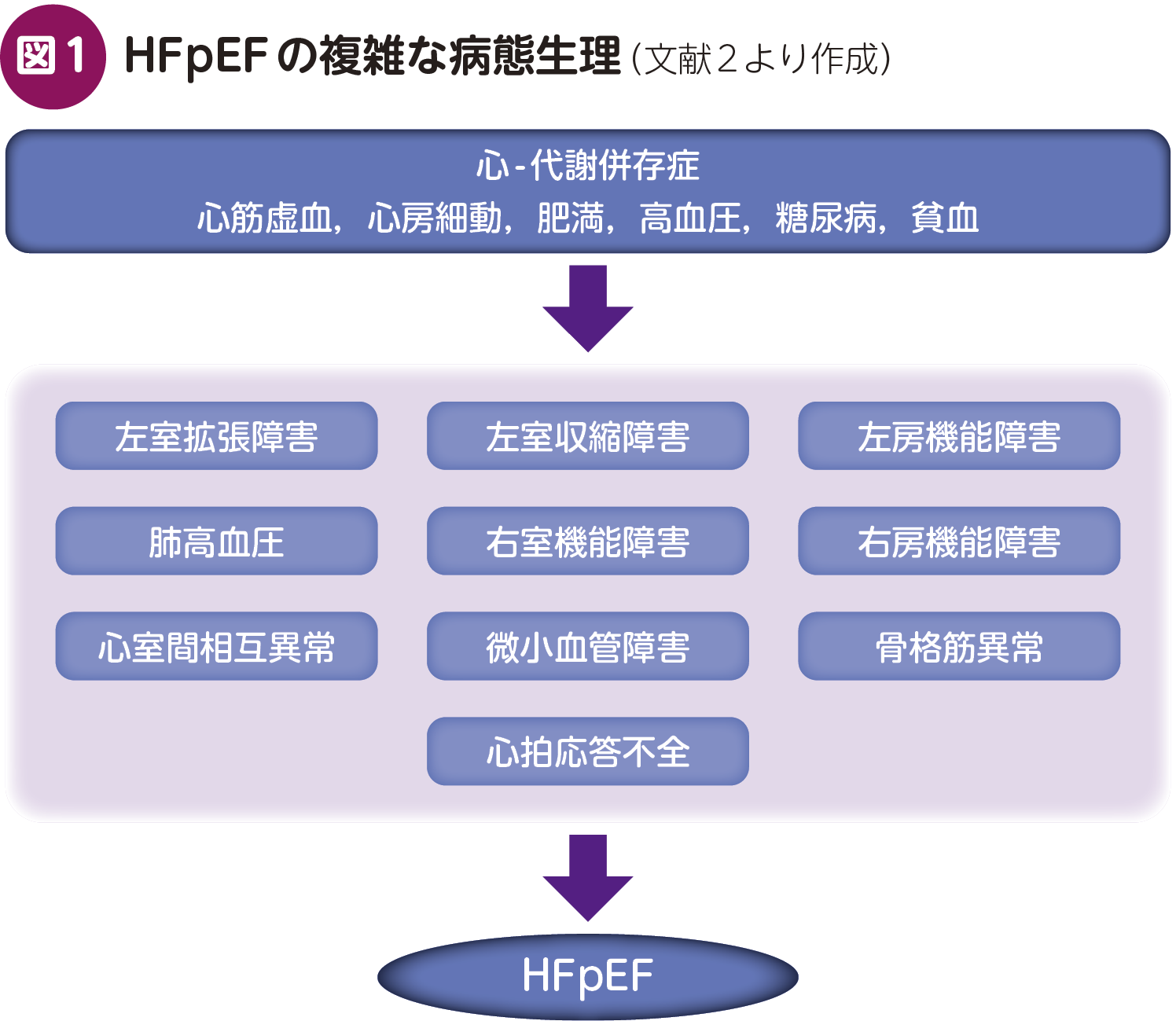
心不全をLVEFで分類する理由は,病態の理解だけではなく,治療戦略の選択に大きく関与するからである。HFrEFにおいては,アンジオテンシン変換酵素阻害薬(ACEi),アンジオテンシンⅡ受容体拮抗薬(ARB),アンジオテンシン受容体ネプリライシン阻害薬(ARNI),β遮断薬,ミネラルコルチコイド受容体拮抗薬(MRA),ナトリウム・グルコース共輸送体-2阻害薬(SGLT-2i)などの薬剤が,複数の大規模臨床試験によって長期予後を改善することが証明されており,HFrEFの標準治療薬として広く用いられてきた。一方で,HFpEFにおいては,長らくうっ血に対する対症療法や,併存症〔高血圧,糖尿病,肥満,心房細動(AF)など〕への対応が中心であり,HFrEFのように明確に生命予後を改善する薬剤は存在しなかった。しかし,2021年にエンパグリフロジン,2022年にダパグリフロジンが,HFpEF患者において心不全による入院および全死亡のリスクを有意に低下させることが報告された。これを契機に,HFpEFに対する薬物治療の開発が進んでおり,これまで以上に適時適切なHFpEF診断の重要性が高まっている。
HFrEFの原因には,陳旧性心筋梗塞や拡張型心筋症などの明確な基礎心疾患が存在することが多いため,HFrEF患者は初診から循環器専門医が関与するケースが多い。これに対してHFpEFは,一目でわかる心機能異常を伴わない症例が多く,その患者の特徴として高齢者,女性,肥満者,高血圧患者,糖尿病患者などが多く含まれるため,一般外来で日常的に診療される患者群に多数潜在している。そのため,HFpEF患者は,まずプライマリ・ケア医が診察する場面が多く,初期の心不全徴候を見逃さずにHFpEFの可能性があると拾い上げることがきわめて重要である。つまり,心不全診療におけるゲートキーパーとして,プライマリ・ケア医が果たす役割は,今後さらに大きくなると考えられる。したがって,本稿では,循環器内科の専門ではない,プライマリ・ケア医が心不全患者を診察する際の一助となることを目的に解説をする。
❷ HFpEFは「心不全パンデミック」の主因である
心不全患者は年々増加しており,本邦において2030年には130万人に達すると予測されている。このような現状は,「心不全パンデミック」と称されるまでに深刻化している1)3)。心不全患者の高齢化が進んでいることに加え,前述の通り,HFpEFの背景には高血圧,AF,冠動脈疾患,糖尿病,肥満などの生活習慣病が多く関与している。これらの要因を反映して,心不全全体に占めるHFpEFの割合は増加しており,現在では全心不全の6割がHFpEFであるとされている。また,心不全患者が増加しているだけではなく,心不全そのものの予後が決して良好ではない点にも留意すべきである。本邦では複数の心不全レジストリーが構築されており,それらのデータによれば,心不全患者の1年以内の全死亡率は約20%と報告されている。心不全による入院患者においては,退院から1年以内に約30%が再入院しており,心不全増悪による再入院から4年間で約半数が死亡するというデータもある。さらに,心不全は医療経済的にも大きな負担をもたらしている。心不全患者1人当たりの年間医療費は約106万円と算出されており,特に心不全による入院では,1回当たり80万円以上の医療費がかかる。これは,患者個人の問題にとどまらず,社会全体に影響を及ぼす公衆衛生上の課題となっている。このように,HFpEFは心不全パンデミックの中心的存在であり,その増加は今後も続くと予想される。したがって,HFpEFを適切に診断・管理し,心不全入院や病態の悪化を防ぐことは,医療現場においてますます重要となっている。

❸ HFpEFの診断はHFrEFに比べると難しい
米国心不全学会/欧州心臓病学会/日本心不全学会が合同で策定し,提唱する「Universal definition and classification of heart failure」によると,「心臓の構造的または機能的異常」による「心不全の症状や徴候」を有し,「脳性ナトリウム利尿ペプチド(BNP)値の上昇」または「心原性の肺うっ血もしくは全身浮腫を示す客観的所見」のいずれか1つが認められた場合に,心不全と診断される(図2)4)。
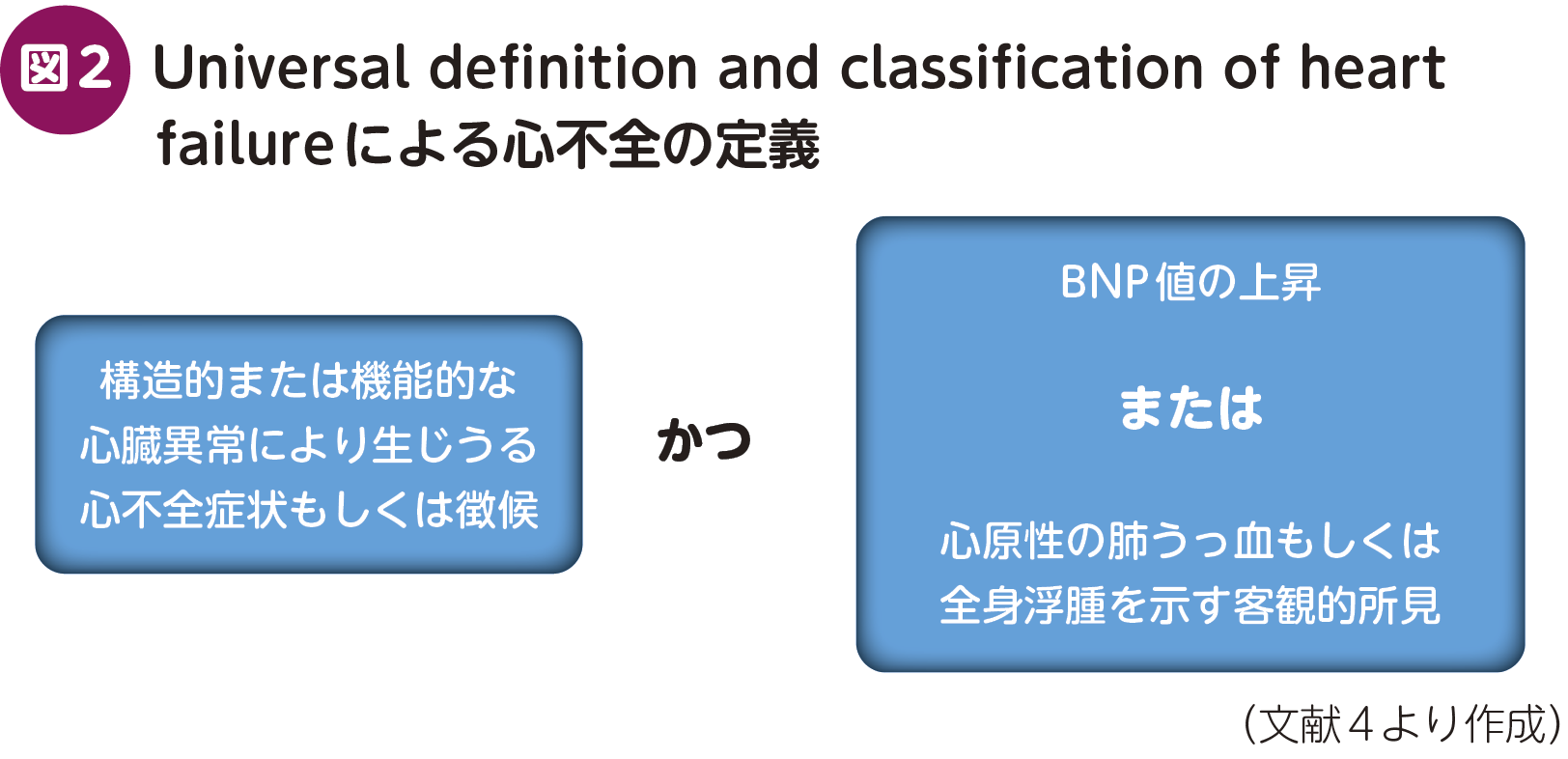
心不全の診断において最も重要な第一歩は,「心不全を疑うこと」である。心不全の症状・徴候で重要なものを表2にまとめた。肺うっ血の症状としては労作時呼吸困難(息切れ)があるが,安静時には無症状のことが多い。夜間に救急搬送されるイメージの多い起坐呼吸や発作性夜間呼吸困難は肺うっ血が重症化した際の症状である。体うっ血に起因する下腿浮腫はよく知られているが,消化管うっ血がある場合には,食思不振や腹部膨満感といった非特異的な訴えを呈し,さらに内服薬の吸収や代謝にも影響を及ぼすことがある。
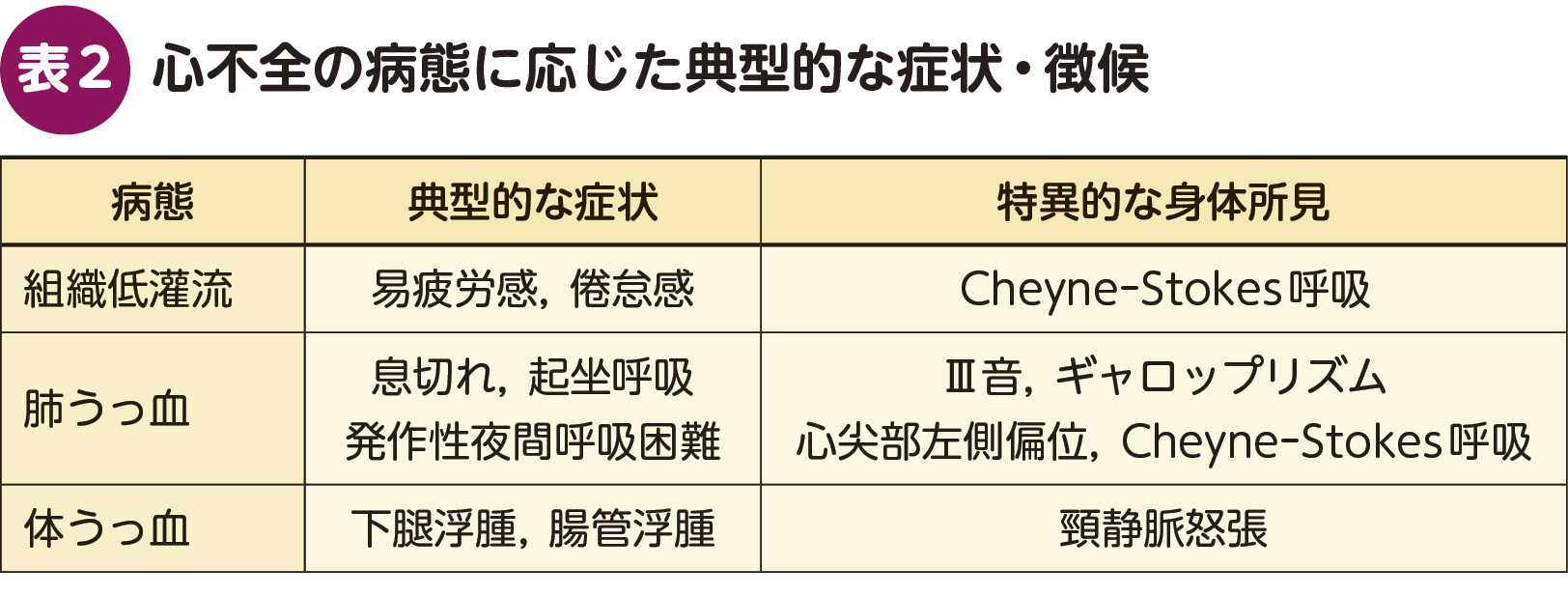
この中で,息切れは心不全を疑うきわめて重要な症状である。そして,BNP値は,心不全における血行動態的特徴のひとつである心内圧上昇を反映する血液マーカーであるため,心不全を疑った場合にはまず測定すべきである5)。「心原性の肺うっ血もしくは全身浮腫を示す客観的所見」が明らかであれば,BNP値の測定がなくとも心不全と診断ができるが,現実の臨床においては,心不全か非心原性肺水腫かの鑑別に苦慮することがしばしばある。これは,特に救急外来などの初期対応において経験されることが多い。
BNP値とその前駆ペプチドNT-proBNP値の2つが測定可能であるが,どちらを測定するかは,施設ごとで採用しているマーカーを用いればよい。ただし,BNP/NT-proBNP値は,心不全以外の因子にも影響を受けることを知っておく必要がある(表3)6)。たとえば,高齢者やAF患者,腎機能が低下している患者では,BNP/NT-proBNP値は高値を示すことが多く,逆に肥満者や心嚢液貯留のある患者では,BNP値が実際の病態に比して低値となることが多い。とりわけ注意が必要なのが,肥満を合併したHFpEF患者である。息切れを主訴に受診し,最終的にHFpEFと診断された患者の中には,BNP値が基準値内に収まっている患者もいる。実際,BNP/NT-proBNP値が正常のHFpEF患者は,HFpEFではない非心原性呼吸困難患者と比較して,予後が不良であるという報告がある7)。したがって,肥満者においては,BNP/NT-proBNP値が正常であっても心不全を完全に否定してはならない。臨床的に心不全を疑う所見がある場合には,画像検査や他の所見と組み合わせた慎重な判断が求められる。







