お知らせ
眼科学[特集:臨床医学の展望2014]
眼科の未来医療として再生医療研究が活気づく
2011年に始まった文部科学省・厚生労働省による再生医療の実現化ハイウェイに端を発し,12年の「成熟細胞が初期化され多能性をもつことの発見」によりノーベル医学・生理学賞を山中伸弥京都大学教授が受賞したことを起爆剤として,日本の再生医療は異次元の世界に踏み込もうとしている。再生医療関連2法が成立し,14年にはいくつかの大型再生医療プロジェクトが臨床研究として試行されようとしている。このような状況において,眼科関連の3課題の再生医療プロジェクトが橋渡し研究として臨床に応用されようとしていることは特筆すべきことである。
また,これらのアイデアと技術がすべて日本独自のものであり,日本の眼科再生医療研究レベルが非常に高度であることを示している。特に,iPS細胞から誘導した網膜色素上皮細胞を用いて加齢黄斑変性(age-related macular degeneration;AMD)を治療しようという試みは他領域からも注目されている。また,培養がほとんど不可能とされていたヒト角膜内皮細胞を十分に細胞機能を保持した状態で培養し,前房という閉鎖空間に注入する培養角膜内皮細胞注入治療法は,眼科領域のみならず他領域にも大いなる示唆を与えるであろう。さらに,iPS細胞から角膜上皮細胞,角膜内皮細胞を分化誘導し,臨床に用いようとするアイデアは,中・長期的に重症角膜疾患患者に福音をもたらすものと思われる。以上のような橋渡し研究が急進展したのが13年である。14年には,現実的な臨床結果が世界に発信されるものと思われる。

さて,眼表面疾患であるドライアイ,中途失明が最も多い疾患である緑内障,中高齢者で急増しているAMDや網膜血管閉塞系の疾患などの治療薬が大きく変化している。いずれも,薬効薬理を十分に考慮して開発された,その効用は大きい。このため,かつては失明の危機にあった患者の多くの視力は保たれるようになってきた。
2013年,特に,ジクアス®,ムコスタ®などのドライアイ治療点眼薬,ザラカム®,デュオトラバ®,コソプト®,アゾルガ®などの抗緑内障配合点眼薬,ルセンティス®,アイリーア®などの抗VEGF(血管内皮増殖因子)薬硝子体内注射が臨床にしっかりと定着することにより,眼科診療が明らかに変化したことは間違いがない。
さらに,角膜移植法におけるDSAEK(descemet’s stripping automated endothelial keratoplasty),DMEK(descemet membrane endothelial keratoplasty)と呼ばれる角膜内皮移植,緑内障手術における緑内障チューブシャントの使用,網膜硝子体手術における硝子体手術機器の精緻化,角膜移植や白内障手術におけるフェムトセカンドレーザーの応用など,外科的アプローチにも大きな改善が見られた。
最後に,眼科における先制医療の試みとして疾患特異的SNPsを解析したいくつかの報告がなされている。その中で重要なものを紹介すると,代表的なものは原発緑内障,特に正常眼圧緑内障(normal tension glaucoma;NTG)でCDKN2B-AS1に関連するSNPsが同定されたことである。このSNPsは世界のすべての人種のNTGに共通してみられることが示された。さらに,AMDの感受性遺伝子が同定され,日本人の眼疾患を伴うスティーブンス・ジョンソン症候群(Stevens-Johnson syndrome;SJS)では,HLA-A0206遺伝子とともにTLR 3やEP3のSNPsを併せ持つことが疾患発症に関与しているという報告がなされ,これらの発見により13年は眼科の先制医療の幕開けとなった。
最も注目されるTOPICとその臨床的意義
TOPIC 1/眼科の再生医療研究が活気づく
社会との関わりが大きい話題としては,眼科の再生医療,特にiPS細胞を用いた加齢黄斑変性(AMD)への治療の準備がほぼできあがったことである。再生医療の実現化という視点でも,AMDという難治性疾患に対する新しい治療法の登場という意味でも注目される。さらに角膜再生医療を含めた展開では,高度技術汎用展開による科学技術立国をめざすという国の方針とも一致する。
この1年間の主なTOPICS
1 眼科の再生医療研究が活気づく
2 日本のドライアイ治療が世界をリードする
3 白内障手術がより精緻化する
4 緑内障治療が多様性を示す
5 網脈絡膜疾患に抗VEGF抗体が幅広く使用される
TOPIC 1▶眼科の再生医療研究が活気づく
眼科から発信しつつある再生医療プロジェクトが注目を集めている。その代表となるのが,国家基幹研究開発推進事業「再生医療の実現化プロジェクト 再生医療の実現化ハイウェイ」に採択された3課題である。このプロジェクトは2011年秋にスタートしたが,当初の採択8課題中,3課題が眼科の再生医療研究である。特に高橋政代氏(理化学研究所)らのグループが自家iPS細胞由来の網膜色素上皮(retinal pigmented epithelium;RPE)細胞を用いて行おうとしている加齢黄斑変性(AMD)治療は,ヒト幹細胞を用いる臨床研究に関する審査委員会でも承認され,13年,マスメディアでも大きな注目を集めた1)。14年中には1例目の臨床例が施行されるはずである。これはiPS細胞のヒトへの応用や,AMDへの再生医療の応用という意味でも大きな第一歩である。
iPS細胞の網膜への応用は,網膜色素変性症(retinitis pigmentosa)などの変性網膜に対する視細胞移植も視野に入れ,いくつかの大きなブレークスルーを経て現実味を増している。また,そのほかの2課題として,当科,同志社大学そして滋賀医科大学が共同研究として行っている角膜内皮障害への体性幹細胞を用いた培養角膜内皮細胞注入治療法2),そして,大阪大学と慶應義塾大学が共同で行っているiPS細胞を用いた角膜再生医療は,日本が発信する世界初の臨床研究(first in man study)に結びつくものである。これら研究の発想,それを支える技術はすべて日本独自のものであり,世界をリードして世界標準化に向けて動いている。このように,2013年は日本の眼科再生医療における記念すべき年であった。
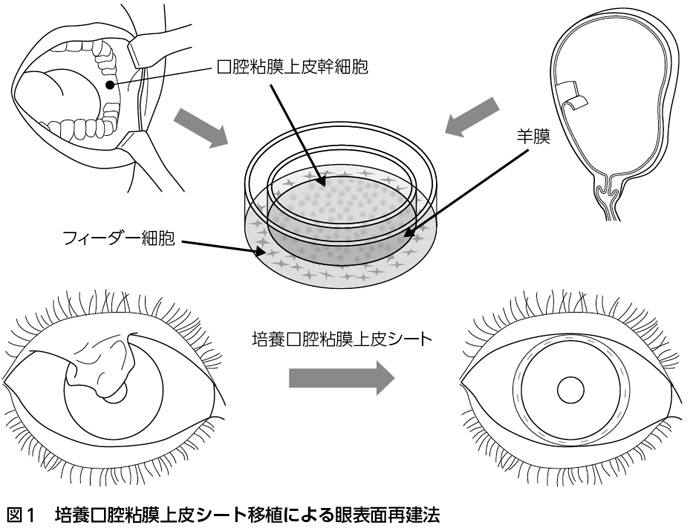
さらに,スティーブンス・ジョンソン症候群(SJS)や化学腐食などの重症眼表面疾患をターゲットにした培養口腔粘膜上皮シート移植については,2つの方法が先進医療Bとして承認されており,臨床現場で最終の評価データを蓄積しつつある。この方法は,2003年頃から日本発の技術として発表されてきたものであり,今まで治療が困難と考えられていた重症眼表面疾患の眼表面を,口腔粘膜上皮を培養して作製した粘膜上皮シートを用いて再建するものである(図1)3)。
◉文 献
1) Kamao H, et al:Stem Cell Reports. 2014; 2(2):205-18.
2) Okumura N, et al:PloS One. 2013;8(2): e58000.
3) Sotozono C, et al:Ophthalmology. 2013; 120(1):193-200.
TOPIC 2▶日本のドライアイ治療が世界をリードする
ドライアイは,眼の不快感に視機能異常を伴う慢性疾患であり,その代表はシェーグレン症候群(Sjögren’s syndrome)である。しかし,近年,VDT(visual display terminals)作業の増加,エアコンなどによる室内の相対湿度の低下,コンタクトレンズ装用による眼表面からの蒸発亢進などにより,涙液が不安定になる軽症から中等症のドライアイ患者が増えており,日本にはおおむね2000万人の患者がいると推定されている。
従来ドライアイは,涙液の異常により引き起こされる角結膜上皮障害と定義されていたが,最近になって,涙液と眼表面上皮には密接な関係があり,その障害として様々なリスクファクターも関与していることが日本発の臨床研究で明らかになってきた。ドライアイの病態生理が明らかになるにつれて,これに対応した新しい作用機序を示す点眼薬が開発され,治療選択肢が広がることが期待されている。
ドライアイ治療には,これまで,ヒアレインⓇ点眼液(ヒアルロン酸ナトリウム,参天製薬)や人工涙液が使用され,重症例には涙点プラグが,炎症例には低濃度ステロイド点眼液が使用されてきた。しかし,2010年12月には,ジクアス点眼液3%(ジクアホソルナトリウム,参天製薬),また12年1月には,ムコスタ点眼液UD2%(レバミピド,大塚製薬)が保険収載され臨床現場に登場し,処方される点眼薬の選択が大きく変化した。ジクアス点眼液3%は,角結膜上皮に存在するP2Y2受容体のアゴニストであり,細胞内カルシウムイオン濃度を上昇させ,結膜上皮からの水分とムチンの分泌を促進する1)。ムコスタ点眼液UD2%は同名称の胃潰瘍予防薬と同様に眼表面のムチン分泌を促進させ,抗酸化,抗アレルギー作用を併せ持つムチン産生促進薬である。いずれも日本独自に開発された新しいタイプの治療薬であり,世界的にも注目されている2)。
2013年,Tear Film Oriented Therapy(TFOT)という考え方がドライアイ研究会から提唱され,涙液の水層,ムチン層,油層のそれぞれをターゲットとする治療概念が定着した。これに伴い,ジクアス点眼液3%とムコスタ点眼液UD2%の有用性がさらに明確に認識され,両者がドライアイへの第一選択の点眼薬として使用されるようになってきた。
◉文 献
1) Takamura E, et al:Br J Ophthalmol. 2012; 96(10):1310-5.
2) Kinoshita S, et al:Ophthalmology. 2013; 120(6):1158-65.
TOPIC 3▶白内障手術がより精緻化する
白内障手術は,加齢などにより混濁した水晶体を超音波破砕装置で破砕・吸引し,代わりに人工的に作製した眼内レンズ(intraocular lens;IOL)を挿入する手術である。この手術において,IOLの飛躍的な進歩および水晶体前嚢と水晶体核を正確に切開するフェムトセカンドレーザーが注目されている。
IOLには単焦点レンズ(monofocal-IOL)と多焦点レンズ(multifocal-IOL)があり,さらに乱視矯正能力を兼ね備えたトーリックレンズがある1)。単焦点レンズは焦点が1箇所であるが,多焦点レンズは遠近両方に焦点があり老視矯正が可能となっている。現在用いられている多焦点レンズは,光を遠方と近方の半分に振り分ける回折型が主流である。トーリックレンズは,半円柱状の球面屈折率を応用した乱視矯正用レンズである。いずれのIOLもアクリル素材の改良などにより,小切開で挿入可能なソフトレンズとして開発されている。白内障手術において,患者の状況に応じてこれらIOLを用いて,乱視や老視も同時に矯正するという考え方がしだいに定着してきたのが2013年の大きな動向である。ただし,多焦点レンズは先進医療あるいは自費診療でないと使用できないという状況に変化はない。
一方,欧米では,フェムトセカンドレーザーを用いて水晶体前嚢と水晶体核を正確に切開する機器が普及しはじめており2),その流れは国内にも徐々に浸透しつつある。このフェムトセカンドレーザーを白内障手術に用いるというコンセプトの一番のポイントは,手術の安全性と精緻性をさらに向上させるところにある。フェムトセカンドレーザーは,数フェムト秒から数百フェムト秒の短いパルスにエネルギーを圧縮して発振するレーザーであり,角膜や水晶体を精度高く切開することができる。実際,フェムトセカンドレーザーを用いた角膜移植は保険承認されている。
このように,白内障手術は光学的な精緻性がさらに求められる時代に向かっており,IOLの手術前度数決定法の精度向上も求められており,光干渉式眼軸長測定器と光線追跡法(レイトレーシング)を用いたOKULIXTMという新しいIOL度数計測ソフトなどが開発されている。
◉文 献
1) Yoshino M, et al:Jpn J Ophthalmol. 2013; Sep 28. [Epub ahead of print]
2) Roberts TV, et al:Ophthalmology. 2013; 120(2):227-33.
TOPIC 4▶緑内障治療が多様性を示す
日本では40歳以上の約5%が緑内障に罹患している。緑内障では高眼圧やそのほかの原因により視神経が障害され,視野狭窄などの症状が生じる。眼圧が正常でも視野障害が生じる緑内障を正常眼圧緑内障(NTG)と称するが,日本人ではこのタイプの緑内障が最も多く,その9割は未診断状態にある。緑内障では視野障害が慢性かつ進行性に生じ,その障害が回復することはない。
緑内障の治療は薬物療法が基本であるが,プロスタグランジン(prostaglandin;PG)製剤,β受容体遮断薬(beta-adrenergic blocking agent),炭酸脱水酵素阻害薬(carbonic anhydrase inhibitor;CAI)など,様々な薬理作用を示す点眼薬があり,緑内障病型,視野進行度,眼圧,全身への影響などに応じて処方される。欧米では異なる作用機序の点眼薬を混合させる配合点眼薬が使用されてきたが,最近になって,日本でも2種類の点眼薬が1つになった抗緑内障配合点眼薬が承認された。2010年からザラカム(キサラタン®+0.5%チモプトール®),デュオトラバ(トラバタンズ®+0.5%チモプトール),コソプト(1%トルソプト®+0.5%チモプトール)が認可され,13年にアゾルガ(1%エイゾプト®+0.5%チモプトール)が承認され,このような配合点眼薬が日常臨床で頻繁に処方されるようになった。ただし,たとえば,チモプトールに代表されるβ遮断系薬剤は全身性の副作用を生じる可能性があり,配合点眼薬の処方では副作用出現に特に注意する必要がある。配合点眼薬の利点としては,2種類を点眼するより点眼回数が減少し,安価なため,患者のアドヒアランスが上がることである。
緑内障治療では,点眼薬による眼圧コントロールが不十分な場合には手術を行う。手術としてはレーザーで周辺虹彩部や隅角部に孔を開けたり,外科的に前房から結膜下に向かう排水路(バイパス)を作成する。従来の手術法では,作成した排水路が術後の癒着などで詰まってしまうことがあった。そこで考案されたのが,チューブを埋め込んで排水路を確保するチューブシャント手術である1)。この緑内障チューブシャントは,欧米では以前から使用されてきたが,日本では未承認状態が続いていた。しかし,2011年にバルベルト®緑内障インプラント(AMO社)とアルコンエクスプレスTM緑内障フィルトレーションデバイス(日本アルコン社)が承認され,13年になってこれらのデバイスが頻繁に使用されるようになった。チューブシャントは,眼内の水(房水)を眼外へ排出させる手術(濾過手術)に用いる排水チューブであり,プレートを持つ長いタイプ(バルベルト)と短いタイプ(エクスプレス)の2種類がある。
◉文 献
1) Gedde SJ, et al:Am J Ophthalmol. 2012; 153(5):789-803.
TOPIC 5▶網脈絡膜疾患に抗VEGF抗体が幅広く使用される
高齢化社会の到来とともに,眼の疾病の中でもAMDが注目されている。AMDは,網膜の中でも中心視力を担っている黄斑部が加齢とともに病的変化を起こす疾患であり,大きく滲出型と萎縮型に分類される。症状が比較的緩やかに進行する萎縮型に比べ,滲出型は,脈絡膜から新生血管が生じることで黄斑部に出血や網膜剥離を起こし,時に急激に視力が低下するため早急な治療が必要である。
この滲出型AMDに対し,2009年にはマクジェン®(ペガプタニブナトリウム,ファイザー)とルセンティス(ラニビズマブ,ノバルティスファーマ)といった抗VEGF薬の硝子体内注射という新しい概念の治療が認可された。この薬剤は,新生血管の成長を促すVEGFを抑えることで新生血管の増殖・成長を妨げ,結果として網脈絡膜出血や滲出性網膜剥離などの病変を改善する。抗VEGF療法の登場により,滲出型AMDの治療目標が視力維持から視力改善へと変化した。
世界各国において滲出型AMD治療の主流となっている抗VEGF療法は,アイリーア(アフリベルセプト,バイエル薬品)という新薬が2012年11月に認可されたことにより,さらに確固たる治療法となった。なお,ルセンティスは13年8月に網膜中心静脈閉塞症(central retinal vein occlusion;CRVO)に伴う黄斑浮腫1),病的近視における脈絡膜新生血管2)にも適応が拡大された。
このように,黄斑疾患にはすべて抗VEGF療法を行うと言っても過言ではない状況になってきた。これも近年,光干渉断層法(optical coherence tomography;OCT)を用いて黄斑部の詳細な断層像を撮影することが可能となり,また黄斑部の自家蛍光像3)などから,黄斑疾患の診断がより精緻に行えるようになったことも一因になっていると思われる。
◉文 献
1) Huang P, et al:PLoS One. 2013;8(12): e82454.
2) Miyake M, et al:Ophthalmology. 2014;121 (1):225-33.
3) Yamagishi T, et al:Ophthalmology. 2012; 119(8):1621-7.