お知らせ
■NEWS ファイザーの経口コロナ治療薬「パキロビッド」を特例承認─入院・死亡リスク89%減少

厚生労働省は2月10日、ファイザーが申請していた経口抗ウイルス薬「パキロビッドパック」(一般名:ニルマトレルビル/リトナビル)を新型コロナウイルス感染症(COVID-19)治療薬として特例承認した。軽症のCOVID-19患者にも使える経口薬の承認は、MSDの「ラゲブリオ」に続き2例目となる。
厚労省はラゲブリオと同じくパキロビッドについても、安定的供給が難しいことから一般流通は行わず、同省が所有した上で、依頼に基づき医療機関・薬局に無償提供する方針だ。

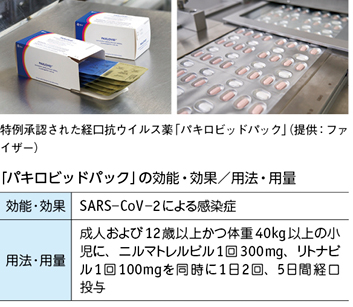
パキロビッドは、ファイザーが新型コロナウイルス(SARS-CoV-2)を標的に創製した新規化合物ニルマトレルビルと、既存の抗ウイルス薬リトナビルの2つの経口薬をパッケージした製品。ニルマトレルビルは、SARS-CoV-2のメインプロテアーゼ(3CLプロテアーゼ)を阻害することでウイルスの複製を抑制。リトナビルは、ニルマトレルビルの代謝(分解)を遅らせ、血漿中濃度を維持する目的で同時に服用する。
パキロビッドは、重症化リスクの高いCOVID-19患者を対象とした国際共同第2/3相試験(EPIC-HR試験)で、プラセボ群に比べ入院・死亡リスクを89%(症状発現から3日以内に投与)ないし88%(5日以内に投与)減少させたとされている。有害事象の発現割合はプラセボ群(24%)と同程度の23%で、概ね軽度だったという。
■投与対象は12歳以上、処方の際は服用中の全薬剤を確認
臨床試験での投与経験を踏まえ、重症化リスク因子を有する12歳以上の軽症~中等症Ⅰの患者が主な投与対象となる。添付文書には、具体的な投与対象については最新のガイドライン(日本感染症学会のガイドライン「COVID-19に対する薬物治療の考え方」)を参考にすることと明記された。
症状発現から6日目以降に投与を開始した患者での有効性を裏付けるデータは得られていないため、症状発現から速やかに投与を開始する。また、高血圧や高脂血症の治療薬など複数の薬剤が併用禁忌とされているため、処方・調剤に当たっては患者が服用中のすべての薬剤を確認する必要がある。