お知らせ
形成外科学[特集:臨床医学の展望2014]
ドナーサイトを犠牲にしない医療の新展開
形成外科は,腫瘍切除や外傷で失われた組織を再建することを得意とする。また,先天的に組織が欠損するような症例(例えば耳介欠損など)を再建することもある。そうした再建には,人工物を用いることもあるが,通常は自家組織を移植することが多い。例を挙げると,舌癌や歯肉癌のような頭頸部癌では,腹直筋皮弁や前外側大腿皮弁に代表される皮膚・皮下脂肪・筋肉を含めた組織移植や,腓骨皮弁のような骨を含めた組織移植を行う。乳癌術後の乳房再建では,腹直筋皮弁や広背筋皮弁のような皮膚・皮下脂肪・筋肉を含めた組織移植を行うことが多い。
マイクロサージャリーの技術や機器の発展もあって,血管吻合の技術を自在に駆使できるようになり,様々な自家組織の移植が可能となった。自家組織移植は腫瘍切除や外傷,あるいは先天性に組織欠損を有するたくさんの人々を救済してきた。しかし一方,自家組織を移植する以上,ドナーサイトを犠牲にするという大きな問題が存在するのも事実である。あるいは非常に大きな組織欠損がある場合,根本的に自家組織移植では対応できないこともある。
そういった問題に対し,主に欧米の形成外科では,ヒトの皮膚,脂肪,筋肉,神経,骨,軟骨などの同種複合組織移植に関する研究が盛んに行われてきた。そして特筆すべきは,すでに実際に顔面や手の同種移植が相当数行われており,それらの長期結果も判明してきていることである。
それに対し我が国の形成外科では,体性幹細胞や前駆細胞に着目した細胞移植医療の研究が盛んに行われてきた。脂肪由来幹(前駆)細胞,骨髄由来幹(前駆)細胞,血管内皮前駆細胞,軟骨前駆細胞,毛包幹細胞などの研究が進んでいる。脂肪由来幹(前駆)細胞や骨髄由来幹(前駆)細胞,血管内皮前駆細胞は血管新生を促進するなどし,難治性創傷の治癒に貢献するとされている。
特に,社会の高齢化に伴い,褥瘡や糖尿病性足潰瘍などの難治性創傷の罹患者数は増加の一途をたどっている。これらの潰瘍の治療は難渋することが多いが,脂肪由来幹(前駆)細胞や骨髄由来幹(前駆)細胞,血管内皮前駆細胞を用いた細胞移植医療が画期的な新治療法として確立される可能性がある。
軟骨前駆細胞を用いた軟骨再生は,小耳症のような軟骨欠損や鞍鼻のような鼻変形などへ応用しうるし,さらには変形性膝関節症のような関節軟骨疾患への応用も模索されている。また,毛包幹細胞を用いた毛包再生は,脱毛症や外傷・腫瘍切除による毛髪欠損への応用が期待される。
最後になるが,2013年の臨床面での最も重要なトピックとしては,2013年7月より乳癌術後の乳房再建にシリコンゲル充塡人工乳房が保険適用されるようになったことが挙げられるであろう。前述したように,乳癌切除後の乳房再建は,これまでは自家組織移植によるもののみが保険適用されていた。ドナーサイトを犠牲にしない再建法が保険適用されたことで,今後,乳房再建は激変する可能性がある。
最も注目されるTOPICとその臨床的意義
TOPIC 1/乳房再建のためのシリコンゲル充塡人工乳房の 保険適用が承認
2013年7月より,乳癌切除後の乳房再建にシリコンゲル充塡人工乳房の使用が保険適用となった。これまでシリコンゲル充塡人工乳房が保険適用でなかったために乳房再建を断念していた人々も数多くおり,そういった人々に大きく門戸を開くことになった。
この1年間の主なTOPICS
1 乳房再建のためのシリコンゲル充塡人工乳房の 保険適用が承認
2 顔面の同種複合組織移植
3 脂肪由来幹(前駆)細胞の形成外科領域への応用
4 軟骨前駆細胞による軟骨再生
5 毛包幹細胞による毛髪再生
TOPIC 1▶乳房再建のためのシリコンゲル充塡人工乳房の保険適用が承認
2012年9月に,乳房再建のためのシリコンゲル充塡人工乳房(ブレスト・インプラント)と,ティッシュ・エキスパンダーと呼ばれる皮膚拡張器が医療機器として承認され,次いで2013年7月より,乳癌切除後の乳房再建においてそれらの使用が保険適用となった。これまで乳房再建で保険適用されている治療法は,自家組織移植によるもののみであった。自家組織移植には常にドナーサイトの犠牲という問題があり,乳房再建を希望するものの,ドナーサイトの犠牲を考え断念する人々も多かった。また,ブレスト・インプラントはすでに一部の施設で保険外では使用されていたが,高額なため経済的な理由で乳房再建を断念するケースもあった。今回のブレスト・インプラントおよびティッシュ・エキスパンダーの保険適用は,そうした人々に大きな福音となるであろう。以下に,現在行われている乳房再建の方法に関して自家組織移植も含めて解説する。
乳房再建には,大きく分けて自家組織を移植する方法と人工物を用いる方法の2つがある。
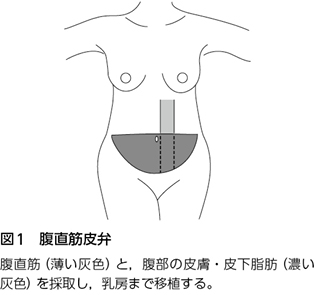
まず自家組織を移植する方法であるが,一般的に行われているのは腹直筋皮弁(図1)と広背筋皮弁(図2)である。両者に共通するのは皮膚・皮下脂肪・筋肉を移植する点である。両者の使い分けは,再建すべき組織のボリュームによりなされる。腹直筋皮弁を採取する下腹部は皮下脂肪が厚く柔らかいことが多く,広背筋皮弁を採取する背部は腹部に比べると皮下脂肪の量は少ない。よって,全乳腺切除例では,再建すべき組織のボリュームが多いため腹直筋皮弁が,逆に乳房温存手術では広背筋皮弁が選択されることが多い。
腹直筋皮弁(図1)は,臍周囲から下腹部に横方向に皮膚・皮下脂肪を採取する。栄養血管は上腹壁動静脈である。皮弁の皮膚・皮下脂肪を栄養する血管(穿通枝)は腹直筋内を走行するため,腹直筋皮弁では腹直筋も含めて採取する。そして,挙上された腹直筋皮弁は,上腹部の皮下トンネルを通して乳房まで移植される。
腹直筋皮弁の問題点は腹直筋を犠牲にすることである。それを改善するために,腹直筋を一部のみ採取する遊離腹直筋皮弁や,腹直筋を採取しない遊離深下腹壁動脈穿通枝皮弁や浅下腹壁動脈皮弁などが開発された。これらは従来の腹直筋皮弁と異なり,マイクロサージャリーの技術を応用し,手術用顕微鏡下に血管吻合を行う。従来の腹直筋皮弁よりも,手術手技としては煩雑で,皮弁を栄養する穿通枝の解剖学的変異も多く難易度が高いが,ドナーサイトの犠牲が少ないため,これらの皮弁を選択する施設も増えてきている。
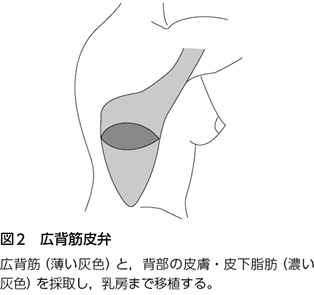
広背筋皮弁(図2)は,背部の広背筋上の皮膚・皮下脂肪を広背筋とともに乳房まで移植する。栄養血管は胸背動静脈である。腹直筋皮弁よりボリュームは少ないが,短時間で移植でき,また皮弁採取後のドナーサイトの機能障害も少ないのが利点である。乳房温存手術に用いられることが多い。
海外ではティッシュ・エキスパンダーやブレスト・インプラントの使用は一般的であるが,我が国ではブレスト・インプラントの使用が保険適用でなかったため,一部の施設での使用に限定されていた。
人工物を用いた乳房再建の最大の利点はドナーサイトの犠牲を生じないことである。乳房再建においては乳腺が切除されているため,人工物は露出を防ぐために大胸筋の下層に挿入される。
通常はブレスト・インプラントの挿入前にティッシュ・エキスパンダーを大胸筋の下層に挿入する。ティッシュ・エキスパンダーは生理食塩水を注入できる構造で,大胸筋の下層で水風船のごとく徐々に膨脹させることができる。そのようにして大胸筋の下層に理想とする大きさのブレスト・インプラントを挿入するためのスペースを作成し,その後2期手術としてブレスト・インプラントの入れ替え手術を行う。すなわち,人工物を用いた乳房再建は通常2回の手術を要する。
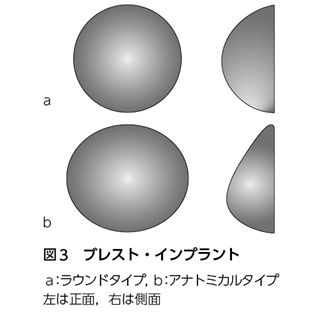
現在,保険適用されているブレスト・インプラントとしてラウンドタイプ(図3a)と呼ばれるお椀形のものがある。この形状のものは比較的小さく下垂の少ない乳房には適しているが,ある程度以上のボリュームのある乳房には使用しにくい。また,乳房の高さのピークが中央よりも尾側にある形状のしずく形のアナトミカルタイプ(図3b)も存在する。乳房の形状を考慮した場合,アナトミカルタイプのほうが乳房再建への適応が広いと考えられる。アナトミカルタイプのブレスト・インプラントも2013年10月11日に医療機器として厚生労働省に承認され,2014年1月8日より保険適用となった。今後,ブレスト・インプラントによる乳房再建はますます増加するであろう。
また,後述する脂肪由来幹(前駆)細胞を用いた細胞移植による乳癌術後の治療が,我が国でも一部の医療機関で開始されてきており,将来この方法が新治療法となる可能性がある。
TOPIC 2▶顔面の同種複合組織移植
腫瘍切除や外傷で失われた組織の再建は,自家組織の移植が今なお主流である。しかし,自家組織の移植はドナーサイトの犠牲という問題を常に伴う。解決策としては,自家組織を使用しない,あるいは使用を最小限にすることが考えられるが,自家組織の移植に代わるものとしては,前述のブレスト・インプラントなどの人工物の使用,ティッシュ・エンジニアリング技術を用いた組織再生や細胞移植医療などが挙げられる。それら以外にはヒトからの同種組織移植も考えられる。実際に欧米では,顔面や手の同種移植が相当数行われており,それらの長期結果も判明してきている1)。
形成外科領域では,ヒトの皮膚,脂肪,筋肉,神経,骨,軟骨といった組織が同種組織移植の対象となりうるが,顔面や手の移植では,それらの組織が単独ではなく複合していることが特徴である。皮膚,骨髄などは抗原性の高い組織であり,移植後の拒絶反応が問題となる。また,免疫反応も筋肉は主に細胞性免疫,皮膚は細胞性と液性免疫の両方などというように,各組織により異なった免疫反応が生じるとされ,同種複合組織移植の成功のためには,すべての組織に対する免疫反応を制御する必要があるとされている2)。しかし,免疫抑制薬の発展もあり,顔面や手といった同種複合組織移植が可能となってきた。
顔面同種移植に関しては2005年のフランスでの第1例以来,2013年までに27例が欧米を中心になされ(図4),フランス,米国,トルコ,スペインでの実施が大半を占めている。顔面の組織欠損に至った原因は,22例が熱傷や銃創,動物咬傷などの外傷,4例は腫瘍,1例は不明である。
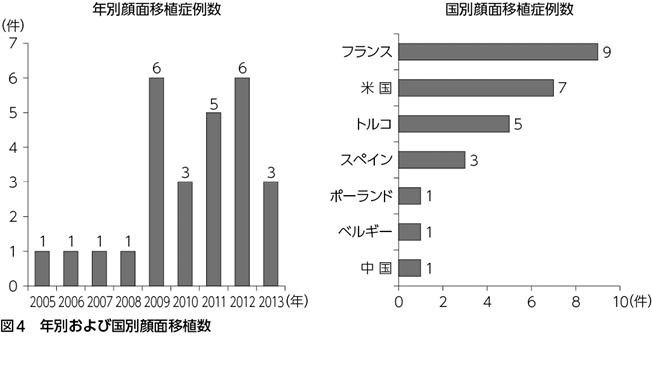
顔面同種移植の結果であるが,知覚神経の回復は早期より良好であるが,運動神経の回復は知覚神経に比べると悪い傾向があるとのことである。ただ,運動神経の部分的な回復は得られるようであり,摂食や笑い,発語の改善が得られている。また,移植時にもともとあった瘢痕組織も切除するため,慢性的な疼痛も減少したとの報告もある。
特筆すべき事項として,2005年の第1例の術後5年の経過報告がある。それによると,移植した粘膜に炎症細胞の浸潤を認めたものの,顔面の機能的および整容的結果は安定していた。また,免疫抑制薬の副作用として,腎機能低下,高血圧,脂質異常,軽度胆管炎,子宮頸部上皮内癌,口唇ヘルペス,口唇伝染性軟属腫などが見られたが,それぞれ免疫抑制薬の変更や円錐切除などで対処可能であったとのことである。
一方,フランスでの7例の顔面移植症例のレビューで,周術期に大量出血,腎不全,急性呼吸促迫症候群,内頸静脈閉塞というような,重篤な合併症を来したとの報告もある。
また,顔面移植後に死亡した症例は27例中3例(11.1%)で,1例は免疫抑制薬を服用しなかったことによると思われる拒絶反応,1例は二次的な下咽頭癌,1例は顔面・両手同時移植を行った症例で移植組織の壊死,感染症で死亡している。今後も国外で顔面移植は引き続き行われていくであろうが,死亡率11.1%という結果を考えると,未だ安全性という点でも改善すべき課題は多い。
◉文 献
1) Siemionow M, et al:Curr Opin Organ Transplant. 2013;18(6):633-9.
2) 柴田 実:日マイクロ会誌. 2007;20(1):3-16.
TOPIC 3▶脂肪由来幹(前駆)細胞の形成外科領域への応用
近年,社会の高齢化に伴い,褥瘡や糖尿病性足潰瘍などの皮膚潰瘍を治療する機会は増加の一途にある。これらは臨床的に非常に難治なことが多く,様々な治療法を駆使しても治癒を得られないことをしばしば経験する。このような難治性創傷に対する画期的な治療法の開発が長年待たれてきた。
そうした中,1997年にAsaharaらにより成人末梢血中に血管内皮前駆細胞が存在することが報告された1)。それまでは難治性創傷の治療は,サイトカインなどの投与により血管新生の促進を目指すものが主体であったが,その発見により細胞移植による難治性創傷の治療という,新たな試みが始まった。その後,血管内皮前駆細胞や骨髄由来幹(前駆)細胞の難治性創傷への応用に関する基礎および臨床研究が多数報告されてきた。
一方,脂肪由来幹(前駆)細胞もその発見以来,研究が飛躍的に発展してきている。特に形成外科では脂肪吸引や皮弁移植時など,もともと脂肪を採取する機会が多い。そのため,細胞移植医療における細胞源として,脂肪由来幹(前駆)細胞は注目されてきた。脂肪由来幹(前駆)細胞は骨髄由来幹(前駆)細胞とよく比較されるが,利点として回収のしやすさ,採取可能な細胞数の多さが挙げられる。脂肪由来幹(前駆)細胞の存在する皮下脂肪は,皮膚の直下にあり採取が非常に容易であるし,同じ組織量から採取できる細胞数は脂肪組織のほうが,骨髄よりも500倍多いとも言われている2)。
脂肪由来幹(前駆)細胞は,脂肪組織中の毛細血管周囲に存在するとされている。脂肪由来幹(前駆)細胞の抽出には,腹部皮下などの脂肪組織を採取し,それを酵素処理し分解した上で遠心分離する。そして得られた細胞群を培養していくと,血管内皮細胞や白血球など,他の細胞が死滅し脂肪由来幹(前駆)細胞が純化される。接着培養が可能であることから,脂肪由来幹(前駆)細胞の大量増殖も容易である3)。
また,脂肪細胞を含まない脂肪由来幹(前駆)細胞や血管内皮細胞,周皮細胞など脂肪組織中の有核細胞の集合体は間質血管細胞群(stromal vascular fraction;SVF)と呼ばれる。脂肪由来幹(前駆)細胞を,接着培養などを経て,純化しなくともSVFの投与で臨床効果が期待できるとされている。実際,すでにSVFの自動分離装置が市販され,我が国での使用も,消化器外科手術に伴う難治性皮膚瘻や乳房温存手術後の乳房変形などで開始されてきている。
難治性創傷における脂肪由来幹(前駆)細胞の臨床応用に関しては,脂肪由来幹(前駆)細胞をin vitroで血管内皮細胞に分化させ,マウス下肢虚血モデルに細胞移植すると血行が改善されたという報告がなされており,新治療法として期待されるところである。また,基礎研究において,移植された脂肪由来幹(前駆)細胞は肝細胞増殖因子(hepatocyte growth factor;HGF)や血管内皮増殖因子(vascular endothelial growth factor;VEGF)などの,血管新生を促進するサイトカインを豊富に産生し分泌するので,血管新生を促進して,難治性創傷の治癒に寄与するとも考えられている。
一方,難治性創傷では,慢性炎症など何らかの原因により,組織の前駆細胞や幹細胞自体が減少しているとも考えられている。そのため,組織の恒常性維持や予備能に障害を生じ,その結果,組織の線維化や虚血を生じ,創傷治癒が遅延するという説もある3)。したがって,減少した前駆細胞や幹細胞を補充し組織の質をという意味でも,脂肪由来幹(前駆)細胞の細胞移植は,簡便で効果の期待しうる方法であると考えられる。
上記以外にも,脂肪由来幹(前駆)細胞は,外傷や腫瘍切除で失われた軟部組織の再建への応用も期待されている。従来,形成外科では脂肪注入という,脂肪組織の移植が行われてきたが,その生着率の低さが問題であった。それに対し,脂肪組織に前述のSVFを加えることにより,脂肪由来幹(前駆)細胞を増加させ,脂肪注入の生着率を上げる試み(cell-assisted transfer)もなされ良好な成績を上げており3),脂肪由来幹(前駆)細胞は軟部組織再建での応用も期待されている。
◉文 献
1) Asahara T, et al:Science. 1997;275(5302) :964-7.
2) 中山享之, 他:日輸血細胞治療会誌. 2013;59 (3):450-6.
3) 吉村浩太郎:医のあゆみ. 2012;242(4):315-20.
TOPIC 4▶軟骨前駆細胞による軟骨再生
先天性の耳介欠損である小耳症の治療としては,現在は肋軟骨移植が行われている。また,外傷性あるいは先天性の鞍鼻変形にも肋軟骨移植が行われることがある。これらの疾患の治療に対しても,自家組織移植によるドナーサイトを犠牲にしない治療法が開発されつつある。すなわち,軟骨前駆細胞を用いた軟骨組織の再生である。
耳介軟骨は弾性軟骨であるが,その軟骨膜に増殖能が高く,多分化能を有する軟骨前駆細胞が存在することが示された。Kobayashiら1)は,in vitroでヒト耳介より採取した軟骨膜細胞は,軟骨細胞よりもきわめて高いコロニー形成能を有し,有意に高い増殖能を持つことを発見した。また,軟骨膜細胞に対し軟骨細胞への分化誘導を行うと,軟骨膜細胞が本来産生するⅠ型コラーゲンの産生は減少し,軟骨細胞のごとくプロテオグリカンとⅡ型コラーゲンを産生するようになり,軟骨細胞に分化した。さらに,軟骨膜細胞は脂肪や骨にも分化でき,多分化能を有することも証明された。
以上から耳介軟骨の軟骨膜の中に高増殖能・多分化能を有する前駆細胞が存在することが判明した。そして,軟骨膜細胞を軟骨分化誘導し,その後,免疫不全マウスの皮下に移植すると,移植3カ月目に軟骨様の組織を形成し,移植後6および10カ月の長期にわたり軟骨様形態を維持した。
また,この軟骨は正常軟骨組織同様に軟骨膜組織も有し,正常軟骨組織と類似した組織を再生できることが示された。今後の臨床応用が期待されるところである。また,Mizunoら2)はイヌの耳介軟骨膜より採取した細胞を膝関節に投与したところ,硝子軟骨である関節軟骨にも分化できることを証明した。こちらも変形性膝関節症のような関節軟骨疾患への応用が待たれる。
◉文 献
1) Kobayashi S, et al:Proc Natl Acazd Sci USA. 2011;108(35):14479-84.
2) Mizuno M, et al:Stem Cells. 2013[Epub ahead of print]
TOPIC 5▶毛包幹細胞による毛髪再生
外傷・腫瘍切除による毛髪欠損や脱毛症に対して,植毛術が行われることがある。しかし,植毛術は自家の頭髪を採取するため,採取量には制限がある。そのため,毛包を増加させる試みなど,様々な毛髪再生の研究が行われてきた。
Toyoshimaら1)2)は,マウス成体頰ひげの毛包上皮性幹細胞と毛包間葉性幹細胞から毛包原基を再生し,ヌードマウス皮膚に移植を行ったところ,74%の頻度で正常の頰ひげと同等の毛の発毛に成功した。また,頰ひげ以外の毛種からも幹細胞を採取して毛包原基を再生し発毛させると,それらは元の毛包から生える毛の性質と一致していた。すなわち,ヒトには頭髪のみならず,眉毛や睫毛など様々なタイプの毛が存在するが,必要とするタイプの毛の再生が可能であることを意味する。
実際にヒトに毛髪を移植する場合は,毛髪の密度も重要である。これに対しては毛包原基を構成する細胞数や移植密度を調節することにより,ヒト頭髪と同等の毛密度を再現できたとのことである。さらに,再生した毛は正常の毛と同様に,毛周期を持ち毛の生え変わりも起こる。また,筋収縮薬には立毛作用もあり,機能的な毛の性質を持ち合わせている。今後のさらなる発展により,男性型脱毛症などへの臨床応用が期待される。
◉文 献
1) Toyoshima KE, et al:Nat Commun. 2012;3: 784.
2) 豊島公栄, 他:理大科学フォーラム. 2013年1月号(No.343), p42-45.